Cyclohexen
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|

| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Cyclohexen | ||||||||||||||||||
| Andere Namen |
1,2,3,4-Tetrahydrobenzol | ||||||||||||||||||
| Summenformel | C6H10 | ||||||||||||||||||
| Kurzbeschreibung |
farblose Flüssigkeit mit phenolartigem Geruch[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 82,15 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
flüssig | ||||||||||||||||||
| Dichte | |||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt |
83 °C[1] | ||||||||||||||||||
| Dampfdruck | |||||||||||||||||||
| Löslichkeit | |||||||||||||||||||
| Brechungsindex |
1,446 (20 °C)[2] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| MAK |
Schweiz: 300 ml·m−3 bzw. 1015 mg·m−3[3] | ||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). Brechungsindex: Na-D-Linie, 20 °C | |||||||||||||||||||
Cyclohexen (1,2,3,4-Tetrahydrobenzol) ist eine farblose Flüssigkeit mit der Summenformel C6H10. Sie gehört zu den Cycloalkenen (cyclische Kohlenwasserstoffe mit mindestens einer Doppelbindung).
Herstellung
[Bearbeiten | Quelltext bearbeiten]Industriell wird Cyclohexen durch Dehydrierung von Cyclohexanol gewonnen. Das Verfahren geht auf den russischen Chemiker Wladimir Nikolajewitsch Ipatjew zurück, welcher den cyclischen Alkohol als Dampf (Gas) über einen erhitzten Feststoffkatalysator aus Tonerde leitete.[4] Bei einer Reaktionstemperatur zwischen 380 und 450 °C entsteht Cyclohexen in 89%iger Ausbeute.[5]

Später wurde gefunden, dass die Dehydratisierung auch ohne Katalysatoren in reinem Wasser unter Druck bei Temperaturen von 250 bis 380 °C möglich ist, wobei 1- und 3-Methylcyclopenten als Nebenprodukte auftreten.[6]
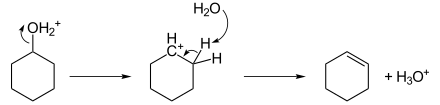
Eine weitere Möglichkeit ist die Dehydratisierung von Cyclohexanol in Gegenwart von konzentrierter Schwefelsäure oder Phosphorsäure.[7] Es handelt sich hierbei um eine säurekatalysierte 1,2-Eliminierung nach dem Mechanismus einer E1-Reaktion.

Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Die farblose Flüssigkeit riecht charakteristisch phenolartig, bei niedrigen Konzentrationen in der Umgebungsluft nach Erdgas. Mit einer Dichte von 0,81 g·cm−3 ist es leichter als Wasser. Die Dämpfe sind sehr viel schwerer als Luft.[1]
Physikalische Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Mit den Methoden der Elektronenbeugung und Mikrowellenspektroskopie wurde die Konformation des Cyclohexens in der Gasphase ermittelt. Es bevorzugt eine Halbsesselkonformation; die Kohlenstoffatome C-3 und C-6 liegen in der Ebene der Doppelbindung.[8] Wie beim gesättigten Kohlenwasserstoff Cyclohexan ist die Konformation flexibel. Das Molekül unterliegt einer Inversion mit einer Inversionsbarriere von ca. 5 kcal/mol (22 kJ/mol). Der Übergangszustand entspricht einer Boot-Konformation.[9]

Chemische Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Die Thermolyse (Pyrolyse) in der Gasphase zwischen 814 bis 902 Kelvin, d. h. 541–629 °C führt in einer unimolekularen Reaktion zu den ungesättigten Kohlenwasserstoffen Ethen und 1,3-Butadien. Dies ist das Ergebnis einer (vermutlich konzertierten) Retro-Diels-Alder-Reaktion.[10][11]

An der C=C-Doppelbindung des Cyclohexens finden für diese Funktion charakteristische Reaktionen statt. Durch Epoxidierung entsteht Cyclohexenoxid. Brom liefert trans-1,2-Dibromcyclohexan. Im ersten Reaktionsschritt wird dabei ein Bromoniumion gebildet, welches ‚auf der Rückseite‘ mit dem freigesetzten Bromidion reagiert.[12] Wie die meisten Cyclohexanderivate liegt trans-1,2-Dibromcyclohexan in einer Sesselkonformation vor, bei der beide Bromatome entweder die equatoriale oder die axiale Position einnehmen (siehe Kasten, rechts).

Ein erster Nachweis von Dichlorcarben gelang durch Addition an die Cyclohexen-Doppelbindung.
Sicherheitstechnische Kenngrößen
[Bearbeiten | Quelltext bearbeiten]Cyclohexen bildet leicht entzündliche Dampf-Luft-Gemische. Die Verbindung hat einen Flammpunkt bei −17 °C.[1][13] Der Explosionsbereich liegt zwischen 1,09 Vol.‑% (37 g/m3) als untere Explosionsgrenze (UEG) und 7,7 Vol.‑% als obere Explosionsgrenze (OEG).)[1] Hier ergibt sich ein oberer Explosionspunkt von −18 °C.[1] Die Grenzspaltweite wurde mit 0,85 mm bestimmt.[1][13] Es resultiert damit eine Zuordnung in die Explosionsgruppe IIB.[1] Die Zündtemperatur beträgt 265 °C.[1][13] Der Stoff fällt somit in die Temperaturklasse T3.
Verwendung
[Bearbeiten | Quelltext bearbeiten]Cyclohexen wird zur Synthese von Adipinsäure und Maleinsäure, einige Derivate zur Herstellung von Arzneimitteln verwendet. Außerdem ist Cyclohexen ein gutes Lösungsmittel in der chemischen Industrie und für Klebstoffe.
Sicherheitshinweise
[Bearbeiten | Quelltext bearbeiten]Cyclohexen ist gesundheitsschädlich. Cyclohexen ist schwach wassergefährdend (WGK 1).[1]
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c d e f g h i j k l m n o p q r s Eintrag zu Cyclohexen in der GESTIS-Stoffdatenbank des IFA, abgerufen am 2. Januar 2024. (JavaScript erforderlich)
- ↑ Datenblatt Cyclohexene bei Sigma-Aldrich, abgerufen am 7. November 2016 (PDF).
- ↑ Schweizerische Unfallversicherungsanstalt (Suva): Grenzwerte – Aktuelle MAK- und BAT-Werte (Suche nach 110-83-8 bzw. Cyclohexen), abgerufen am 2. November 2015.
- ↑ W. Ipatiew: Katalytische Reaktionen bei hohen Temperaturen und Drucken. XX. Dehydration cyclischer Alkohole. In: Berichte der deutschen chemischen Gesellschaft, 1910.
- ↑ Louis F. Fieser, Mary Fieser: Lehrbuch der Organischen Chemie, Übersetzt und bearbeitet von Hans R. Hensel, Verlag Chemie, Weinheim 1954, S. 58.
- ↑ Naoko Akiya, Phillip E. Savage: Kinetics and Mechanism of Cyclohexanol Dehydration in High-Temperature Water. In: Industrial & Engineering Chemistry Research Jg. 2001 Bd. 40, Heft 8, S. 1822–1831. DOI: 10.1021/ie000964z
- ↑ Siegfried Hauptmann: Organische Chemie, 1. Auflage, S. 243, Verlag Harry Deutsch, Thun 1985.
- ↑ Joseph F. Chiang, Simon Harvey Bauer: Molecular structure of cyclohexene. In: Journal of the American Chemical Society Jg. 1969, Bd. 91, Heft 8, S. 1898–1901. DOI: 10.1021/ja01036a004
- ↑ Ernest L. Eliel, Samuel H. Wilen, Lewis N. Mander: Stereochemistry of Organic Compounds, John Wiley & Sons, 1994, ISBN 0-471-01670-5
- ↑ Masao Uchiyama, Tadao Tomioka, Akira Amano: Thermal Decomposition of Cyclohexene. In: The Journal of Physical Chemistry Jg. 1964, Bd. 68, Heft 7, S. 1878–1881. DOI: 10.1021/j100789a036
- ↑ D. C. Tardy, R. Ireton, A. S. Gordon: Thermal decomposition of labeled cyclohexene. A complex reaction involving a forbidden 1,2-hydrogen elimination. In: Journal of the American Chemical Society, Jg. 1979, Bd. 101, Heft 6, S. 1508–1514. DOI: 10.1021/ja00500a024
- ↑ Siegfried Hauptmann: Organische Chemie, 1. Auflage, S. 233, Verlag Harry Deutsch, Thun 1985.
- ↑ a b c E. Brandes, W. Möller: Sicherheitstechnische Kenngrößen. Band 1: Brennbare Flüssigkeiten und Gase. Wirtschaftsverlag NW – Verlag für neue Wissenschaft, Bremerhaven 2003.



