Basalganglien

Als Basalganglien oder Nuclei basales werden mehrere unterhalb der Großhirnrinde (Cortex cerebri) liegende Kerne bzw. Kerngebiete des Endhirns (Telencephalon), Zwischenhirns (Diencephalon) und Mittelhirns (Mesencephalon) zusammengefasst. Diese subkortikalen basalen Kerne sind für wichtige funktionelle Aspekte motorischer, kognitiver und limbischer Regelungen von großer Bedeutung, beispielsweise für Spontaneität, Affekt, Initiative, Willenskraft, Antrieb, schrittweises Planen, vorwegnehmendes Denken, Erwartungen, motorische Selektion.
Anatomie
[Bearbeiten | Quelltext bearbeiten]

Zu den Basalganglien, teilweise auch als Stammganglien oder nach neuerer Nomenklatur als Basalkerne (Nuclei basales) bezeichnet, zählt man im engeren Sinne (anatomisch):
- den Nucleus caudatus (geschweifter Kern) und
- den Nucleus lentiformis (linsenförmiger Kern). Dieser besteht aus:
Nucleus caudatus und Putamen liegen in der frühen Embryonalentwicklung zusammen und werden dann durch das Durchwachsen der Capsula interna, der längsten Projektionsbahn des Zentralen Nervensystems, getrennt. Sie bleiben jedoch über feine Streifen bzw. Brücken grauer Substanz (Pontes grisei caudatolenticulares) verbunden und werden daher zusammen als Striatum (das Gestreifte) bezeichnet. Diese Zusammenfassung ist nicht nur morphologisch, sondern auch funktionell relevant. Ventral sind Nucleus caudatus und Putamen noch verbunden. Diese Stelle wird als „Fundus striati“ oder Nucleus accumbens bezeichnet.
Zu den Basalganglien im weiteren Sinne (funktionell) rechnet man:
- die Substantia nigra (schwarze Substanz), ein im Mittelhirn gelegenes Kerngebiet bestehend aus
- Pars compacta (SNc)
- Pars reticularis (SNr) und lateralis
- den Nucleus subthalamicus (STN, auch Corpus Luysi genannt).
Die Eingangsstation in die Basalganglien stellt das Striatum dar. Es erhält nicht nur Projektionen aus der Großhirnrinde und der Substantia nigra, sondern noch aus den verschiedensten Kerngebieten des Zentralnervensystems, z. B. Raphe-Kerne, Formatio reticularis. Den Ausgangspunkt bildet das Pallidum internum (GPI), welches direkt GABAerg (hemmend) auf den Thalamus projiziert und ihn (und somit auch die Großhirnrinde) hemmt. Sowohl Pallidum als auch Nucleus subthalamicus gehören entwicklungsgeschichtlich zum Thalamus ventralis.
Funktion
[Bearbeiten | Quelltext bearbeiten]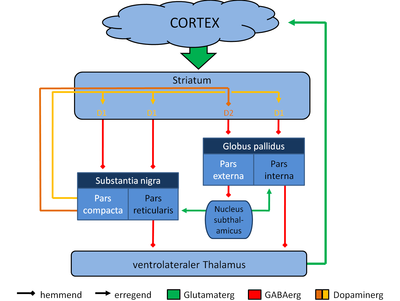
Über die bis heute nur ansatzweise verstandene komplexe Funktion der Basalganglien wird gegenwärtig hypothetisch postuliert, dass sie maßgeblich sowohl an der Selektion und Prozessierung von derzeit erforderlichen „motorischen“ und „nicht-motorischen“ (höher-integrativen) Handlungsmustern beteiligt sind als auch gleichzeitig an der Suppression bzw. Inhibition derzeit nicht geforderter, also unerwünschter und damit zu unterdrückender Aktivierungsmuster. Die Basalganglien sind gewissermaßen als ein Filterprozess (siehe Gating) in eine komplexe Regelschleife (loop) eingebunden, die von der Großhirnrinde ausgeht und über die Basalganglien und den Thalamus zurück zum Großhirn (Frontallappen) verläuft. Von fast der gesamten Großhirnrinde, genauer von den Nervenzellen der Schicht V, gelangen bis auf wenige Ausnahmen (primärer visueller und auditiver Cortex) Informationen zum Striatum als der Eingangsstation der Basalganglien in Form kortiko-striataler Verbindungen (exzitatorische glutamaterge Transmission). Über die Ausgangsstation der Basalganglien, die Substantia nigra (Pars reticulata SNR) und den Globus pallidus internus (GPI), gelangt die von den Basalganglien verarbeitete Endinformation (inhibitorisch GABA-erge Transmission) zum Thalamus und vom Thalamus (exzitatorischer, glutamaterg) primär zur frontalen Hirnrinde zurück. Die Basalganglien stellen einen elementaren, im Detail noch wenig verstandenen funktionellen Beitrag für den frontalen, sogenannten exekutiven Teil des Gehirns dar.
Man grenzt heute eine direkte (exzitatorische) Verbindung vom Striatum zu den Ausgangsstrukturen (SNR und GPI) gegenüber einer indirekten (inhibitorischen) Verbindung ab. Das Striatum und der GPI sind beide GABAerg (hemmend). Somit führt eine direkte Projektion des Striatum auf den GPI zu einer Hemmung seiner Hemmung (Disinhibition), was nun eine Erregung des Thalamus bzw. der Großhirnrinde bedeutet. Bei der indirekten Verbindung ist es etwas komplizierter: Das Striatum hemmt den Globus pallidus externus, GPE, welcher den Nucleus subthalamicus hemmt. Somit kommt es wieder zu einer Hemmung der Hemmung, sprich der Nucleus subthalamicus ist erregt. Er wirkt nun wiederum erregend auf den GPI, welcher nun den Thalamus und somit indirekt die Großhirnrinde hemmt. Wenn der GPE gehemmt wird, verschwindet auch eine direkte Hemmung auf den GPI, was die inhibitorische Wirkung des GPI noch mehr verstärkt. Hierdurch liegt die Ausgangsmodulation der Basalganglienaktivität sozusagen an zwei entgegengesetzt gerichteten Zügeln, die ein mehr (Plus) oder weniger (Minus) an Bewegung oder Handlungsmustern (im weiteren Sinne „Verhalten“) bewirken.
Die von den Nervenzellen der Substantia nigra (Pars compacta) ausgehende dopaminerge Projektion zum Striatum stellt heute deswegen einen besonders stark erforschten Modulationsweg innerhalb der Basalganglien dar, weil man erkannt hat, dass seine Störung infolge einer vorzeitigen Degeneration („Alterung“) zu den Symptomen der Parkinsonschen Krankheit führt.
Krankheiten
[Bearbeiten | Quelltext bearbeiten]Zu den neurologischen Krankheiten, die mit einer Funktionsstörung der Basalganglien einhergehen, gehören:
- Parkinson-Syndrome, z. B. Parkinson-Krankheit, Multisystematrophie (MSA)
- Neurodegeneration mit Eisenablagerung (NBIA), z. B. Hallervorden-Spatz-Syndrom
- Dystonie-Syndrome, z. B. Torticollis spasmodicus, Athetose, Tardive Dystonie
- Choreatische Syndrome, z. B. Chorea Huntington, Hemiballismus, Tardive Dyskinesie, Choreoathetose
- PANS/PANDAS
- ADHS
- Tic-Störungen, z. B. Tourette-Syndrom
Beim „Morbus Parkinson“ kommt es infolge einer chronisch fortschreitenden Degeneration der von der Substantia nigra, Pars compacta (SNc) ausgehenden dopaminergen Transmission zu einer pathologischen Veränderung der striatalen Modulation, die in sehr unterschiedlichem Ausmaß zu Muskeltonusveränderungen (Rigor), Bewegungsverarmung (Hypokinese), Zittern (Tremor), Haltungsinstabilität, vermindertem Geruchssinn (Hyposmie) und anderen Symptomen führen kann.
Bei frühkindlichen, perinatalen Hirnschädigungen (z. B. Kernikterus, Sauerstoffmangel) sind Schädigungen der Basalganglien mit Veränderungen des Muskeltonus (z. B. Athetose) häufig, auch als Status marmoratus bezeichnet. Bei Morbus Wilson kommt es durch Kupferablagerung u. a. in den Basalganglien zu komplexen motorischen und psychischen Funktionsstörungen.
Gating-Theorie
[Bearbeiten | Quelltext bearbeiten]Wie oben beschrieben, wird die Filterfunktion der Basalganglien, bzw. des Striatum als Gating bezeichnet. Die Gating-Theorie an sich ist neuroanatomisch und -physiologisch relativ gut etabliert, findet sich jedoch unter diesem Namen zurzeit fast nur in neuropsychologischen Publikationen. Dies ist für die Validität der Gating-Theorie ausgesprochen wichtig, da Gating an sich inhaltlich nichts Neues darstellt, sondern nur einen anderen Namen für ein bereits bestehendes Konzept.
Aus der Gating-Theorie lässt sich eine Reihe von anderen Theorien ableiten, Krankheiten erklären und interindividuelle Unterschiede bezüglich der Persönlichkeit des Menschen beschreiben:
- Tic-Störungen als Fehlverschaltung der Basalganglien, bei denen ein immer wiederkehrendes Bewegungsmuster ausgeführt wird, indem gewisse Verhaltenspläne durch das Striatum falsch prozessiert werden.
- ADHS: Hier vermuten manche Forscher ähnliche Verschaltungsmuster wie bei Tic-Störungen, nur dass in diesem Falle nicht ein bestimmtes Verhaltensmuster falsch prozessiert würde, sondern eine generelle inadäquate Filterfunktion vorliegt, in der redundantes oder „unangebrachtes“ Verhalten erregt wird (Hyperaktivität), während neue Verhaltenspläne fehlerhaft gehemmt werden (Aufmerksamkeitsdefizit).
- Zwangsstörung: Die Gating-Theorie der Zwangsstörungen ist vergleichbar mit der der Tic-Störungen, wobei sie wissenschaftlich und auch nach Meinung vieler Fachleute eher „auf wackeligen Beinen“ steht, da sie zwar Zwangshandlungen erklären kann, jedoch weder Zwangsgedanken, noch die affektive Komponente der Zwangsstörung.
Ein weiterer Erklärungsansatz aus der Gating-Theorie ist der der interindividuellen Persönlichkeitsunterschiede: Hans Jürgen Eysenck beschrieb einen der bis heute etabliertesten Persönlichkeitsfaktoren als Extraversion vs. Introversion und erklärte ihn über kortikale Grunderregung. Diese neurophysiologische Erklärung wird jedoch mittlerweile immer häufiger hinterfragt. Neuere Forschung versucht, diese Persönlichkeitsdimension über das Gating zu erklären. Demnach haben Introvertierte ein effizienteres Gating im Vergleich zu Extravertierten, weshalb Extravertierte ihr Gating (also die Fähigkeit des Striatums, Verhaltenspläne adäquat zu prozessieren) verstärken müssen, indem sie zusätzliche internale oder externale sensorische Stimuli suchen. Hierdurch wird, nach der Theorie, die glutamaterge Projektion der Hirnrinde auf das Striatum verstärkt, wodurch dieses nun besser filtern kann. Diese Theorie erklärt beispielsweise, warum Extravertierte besser Lernen, wenn sie z. B. Musik hören, während Introvertierte hierdurch eher abgelenkt werden.
Die Gating-Theorie im weiteren Sinne ist vielversprechend, steckt jedoch zurzeit noch in ihren Anfängen. Viele der Subtheorien sind wissenschaftlich fundiert, wobei die Verknüpfungen teilweise (obwohl logisch) noch schlecht bis gar nicht untersucht sind.
Quellen
[Bearbeiten | Quelltext bearbeiten]- Jonathan W. Mink: The Basal Ganglia Kapitel 31 – Fundamental Neuroscience 2003 Academic Press
- Bastian Conrad, Andres Ceballos-Baumann: Bewegungsstörungen in der Neurologie – richtig erkennen und behandeln. 1. Auflage. Thieme Verlag, Stuttgart/New York 1996, ISBN 3-13-102391-0.
- Andres Ceballos-Baumann, Bastian Conrad: Bewegungsstörungen. 2. Auflage. Thieme Verlag, Stuttgart/New York 2005, ISBN 3-13-102392-9.
- G. Percheron, G. Fénelon, V. Leroux-Hugon, A. Feve (1994): Histoire du système des ganglions de la base. La lente émergence d’un système cérébral majeur. Revue Neurologique Aug-Sep; 150(8-9):543-54.
- Lennart Heimer: The Human Brain and Spinal Cord: Functional Neuroanatomy and Dissection Guide. Springer, New York 1995, ISBN 0-387-94227-0.
Weblinks
[Bearbeiten | Quelltext bearbeiten]- Models of Basal Ganglia. In: Scholarpedia. (englisch, inkl. Literaturangaben)
- Mit den Basalganglien assoziierte Funktionen und Erkrankungen mit Links zu aktuellen Studien