o-Toluidin
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|

| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | o-Toluidin | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C7H9N | ||||||||||||||||||
| Kurzbeschreibung |
farblose bis rotbraune Flüssigkeit mit charakteristischem Geruch[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 107,16 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
flüssig[1] | ||||||||||||||||||
| Dichte |
1,00 g·cm−3[1] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt |
200 °C[1] | ||||||||||||||||||
| Dampfdruck | |||||||||||||||||||
| pKS-Wert |
4,44 (der konjugierten Säure BH+)[2] | ||||||||||||||||||
| Löslichkeit |
wenig löslich in Wasser (15 g·l−1 bei 20 °C)[1] | ||||||||||||||||||
| Brechungsindex |
1,5728[3] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Zulassungsverfahren unter REACH |
besonders besorgniserregend: krebserzeugend (CMR)[5] | ||||||||||||||||||
| MAK |
Schweiz: 0,1 ml·m−3 bzw. 0,5 mg·m−3[6] | ||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). Brechungsindex: Na-D-Linie, 20 °C | |||||||||||||||||||
o-Toluidin ist eine chemische Verbindung aus der Gruppe der aromatischen, einfach methylierten Aniline und Toluidine. Es ist isomer zu m-Toluidin und p-Toluidin.
Gewinnung und Darstellung
[Bearbeiten | Quelltext bearbeiten]Alle drei isomeren Toluidine werden aus Nitrotoluolen (aus Toluol durch Nitrierung zugänglich) durch Reduktion hergestellt. Die Reduktion kann zum einen mit Eisen, Essigsäure und Salzsäure durchgeführt werden (Béchamp-Reduktion). Heute überwiegt die katalytische Hydrierung mit Raney-Nickel. Als Lösungsmittel werden hier oft niedere, aliphatische Alkohole (Methanol, Ethanol, n-Propanol oder iso-Propanol) eingesetzt. Die Hydrierung findet in der Regel bei Drücken zwischen 3 bar und 20 bar H2-Druck (sog. Niederdruckhydrierung) oder bei 20 bis 50 bar (sog. Mitteldruckhydrierung) statt.
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]o-Toluidin ist eine farblose, sich an Luft und Licht allmählich rotbraun färbende, schwer entzündliche, wenig flüchtige Flüssigkeit mit charakteristischem Geruch, die wenig löslich in Wasser ist. Sie hat eine Leitfähigkeit von 3,792 × 10−5–S/m bei 25 °C und einen pH-Wert von 7,4 bei 20 °C und einer Konzentration von 1,4 Masse-%.[1]
Alle Toluidine sind schwache Basen, ihre (pKs-Werte) liegen in der gleichen Größenordnung wie Anilin (4,603).[2]
Die Dampfdruckfunktionen ergeben sich nach Antoine entsprechend log10(p) = A−(B/(T+C)) (p in bar, T in K) wie folgt:
| Typ | T in K | A | B | C |
|---|---|---|---|---|
| o-Toluidin[7] | 391,6–473,4 | 4,19168 | 1617,232 | −87,126 |
| m-Toluidin[7] | 394,9–476,5 | 4,19983 | 1618,386 | −90,631 |
| p-Toluidin[8] | 315–473,5 | 4,71884 | 1961,716 | −57,0 |
Verwendung
[Bearbeiten | Quelltext bearbeiten]Die Toluidine hatten früher fast ausschließlich als Zwischenprodukte zur Herstellung von Farbstoffen und Pigmenten sehr große Bedeutung. Mittlerweile werden auch einige Herbizide auf Basis dieser Verbindungen hergestellt. o- und p-Toluidin sind wichtige Ausgangsstoffe zur Herstellung von Chlortoluidinen und nitrierten Toluidinen. Diese dienen, neben den Toluidinsulfonsäuren, zur Herstellung von Pharmazeutika, Farbstoffen und Pigmenten.
Über eine Diazotierung (und anschließende „Verkochung“) können aus den Toluidinen die Kresole erhalten werden.
o-Toluidin ist Ausgangsstoff zur Herstellung der Kupplungskomponente Naphtol AS-D. Wichtige Azofarbstoffe auf Basis von o-Toluidin sind Acid Red 24 (C.I. 16140), Solvent Red 26 (C.I. 26120) und Solvent Yellow 3 (C.I. 11160). Es hat auch als Vorprodukt für die Herbizide Phenmedipham und Chlordimeform Bedeutung.
| Chemische Struktur | Name | Verwendung |
|---|---|---|
 |
6-Chlor-2-methylanilin | für Pharmazeutika |
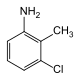 |
3-Chlor-2-methylanilin | als Diazo-Komponente für Naphtol-AS-Entwicklungsfarbstoffe,
Ausgangsstoff für 2,6-Dichlortoluol |
 |
4-Chlor-2-methylanilin | Diazo-Komponente für Naphtol-AS-Entwicklungsfarbstoffe,
Vorprodukt für Indigo- und Thioindigofarbstoffe, Ausgangsstoff für 2,5-Dichlortoluol |
 |
5-Chlor-2-methylanilin | Diazo-Komponente für Naphtol-AS-Entwicklungsfarbstoffe |
 |
2-Aminotoluol-4-sulfonsäure | als Diazo-Komponente für Azofarbstoffe |
 |
2-(Ethylamino)-toluol-4-sulfonsäure | zur Herstellung von Farbstoffen |
 |
2-Aminotoluol-5-sulfonsäure | als Diazo-Komponente für Azofarbstoffe |
 |
2-Amino-3-chlortoluol-5-sulfonsäure | Zwischenprodukt zur Herstellung von Pyrazolonfarbstoffen,
z. B. Acid Yellow 18, C.I. 19020 |
 |
2-Amino-6-chlortoluol-3-sulfonsäure | Zwischenprodukt für Azofarbstoffe |
 |
2-Amino-6-chlortoluol-4-sulfonsäure | Zwischenprodukt für Azofarbstoffe,
z. B. Acid Brown 105, C.I. 13530 |
Sicherheitshinweise
[Bearbeiten | Quelltext bearbeiten]Die Dämpfe von o-Toluidin können mit Luft ein explosionsfähiges Gemisch (Flammpunkt 85 °C, Zündtemperatur 480 °C) bilden. Sie greift verschiedene Kunststoffe an.[1] Es darf nach reduktiver Spaltung von Azogruppen nicht von Textilien oder Ledererzeugnissen, die längere Zeit mit der menschlichen Haut direkt in Berührung kommen, freigesetzt werden (Anlage 1 der Bedarfsgegenständeverordnung).
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c d e f g h i j k l m n Eintrag zu o-Toluidin in der GESTIS-Stoffdatenbank des IFA, abgerufen am 20. Januar 2022. (JavaScript erforderlich)
- ↑ a b Zvi Rappoport (Hrsg.): CRC Handbook of Tables for Organic Compound Identification. 3rd Edition, CRC Press/Taylor and Francis, Boca Raton, FL, 1967, ISBN 0-8493-0303-6, Acid Dissociation Constants of Organic Bases in Aqueous Solution, S. 437.
- ↑ J.S. Bowers, Jr.: Toluidines in Ullmann’s Encyclopedia of Industrial Chemistry, 2012 Wiley-VCH Verlag GmbH & Co. KGaA, Weinheim, doi:10.1002/14356007.a27_159.
- ↑ Eintrag zu o-toluidine im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- ↑ Eintrag in der SVHC-Liste der Europäischen Chemikalienagentur, abgerufen am 15. Juli 2014.
- ↑ Schweizerische Unfallversicherungsanstalt (Suva): Grenzwerte – Aktuelle MAK- und BAT-Werte (Suche nach 95-53-4 bzw. O-Toluidin), abgerufen am 2. November 2015.
- ↑ a b R. R. Dreisbach, S. A. Shrader: Vapor Pressure–Temperature Data on Some Organic Compounds. In: Ind. Eng. Chem. Band 41, Nr. 12, 1949, S. 2879–2880, doi:10.1021/ie50480a054.
- ↑ Daniel R. Stull: Vapor Pressure of Pure Substances. Organic and Inorganic Compounds. In: Ind. Eng. Chem. Band 39, Nr. 4, 1947, S. 517–540, doi:10.1021/ie50448a022.


