Rachitis
| Klassifikation nach ICD-10 | |
|---|---|
| E55.0 | Floride Rachitis |
| E64.3 | Folgen der Rachitis |
| E83.30 | Familiäre hypophosphatämische Rachitis |
| E83.31 | Vitamin-D-abhängige Rachitis |
| N25.0 | Renale Rachitis |
| ICD-10 online (WHO-Version 2019) | |

Die Rachitis (auch Rhachitis, von altgriechisch ῥάχις rháchis „Rücken, Rückgrat“), auch Englische Krankheit oder Rickets genannt, ist eine meist mit Vitamin-D-Mangel verbundene Erkrankung des wachsenden Knochens mit gestörter Mineralisation der Knochen und Desorganisation der Wachstumsfugen bei Kindern. Das der Rachitis entsprechende Krankheitsbild im Erwachsenenalter ist die Osteomalazie.
Rachitis ist auf eine ungenügende Konzentration des Calcium-Phosphat-Produktes im Blut zurückzuführen und die dadurch verursachten hormonellen Gegenregulationsmechanismen. Die häufige Calciummangel-Rachitis wird meist durch eine erworbene Vitamin-D-Stoffwechselstörung oder eine mangelnde Calciumaufnahme mit der Nahrung hervorgerufen. Sie wird von der seltenen Phosphatmangel-Rachitis unterschieden, die durch einen zumeist vererbten übermäßigen Phosphatverlust über die Nieren verursacht wird. Zu den Symptomen gehören neben Wachstumsstörungen mit Verformungen der Knochen insbesondere Auftreibungen der Knorpel-Knochen-Grenzen an den Wachstumsfugen. Die Behandlung richtet sich nach der Ursache. Sie besteht in einer Ergänzung von Vitamin D, gegebenenfalls zusätzlich von Calcium oder Phosphat. Zur Prophylaxe ist es üblich, Säuglingen während des ersten Lebensjahres Vitamin D in einer täglichen Einzeldosis zu verabreichen.
Häufigkeit
[Bearbeiten | Quelltext bearbeiten]Da die Rachitis keine meldepflichtige Erkrankung ist, gibt es kaum Zahlen über die Erkrankungshäufigkeit. Ein Expertengremium des amerikanischen Center for Disease Control hat die Häufigkeit einer Krankenhausbehandlung wegen Rachitis mit neun von einer Million Kindern ermittelt. Eine ambulante Rachitis-Therapie wurde im gleichen Bericht mit einer Häufigkeit zwischen 23 und 32 je einer Million Kindern angegeben. In diesem Kollektiv waren afro-amerikanische Kinder mit drei Vierteln der stationären und 100 % der ambulanten Fälle mit Abstand am häufigsten betroffen.[1] Ein subklinischer Vitamin-D-Mangel noch ohne klinische Symptome einer Rachitis wird selbst in hochentwickelten Ländern sehr viel häufiger gefunden. In amerikanischen Untersuchungen hatten 80 % der Neugeborenen und am Ende des Winters fast die Hälfte der Mädchen im Alter zwischen neun und elf Jahren verringerte Vitamin-D-Konzentrationen im Blut. Selbst in Ländern mit hoher Sonneneinstrahlung tritt Vitamin-D-Mangel epidemisch auf, z. B. wenn Frauen aus religiösen Gründen eine Burka tragen.[2] In Europa kommt eine Rachitis vermehrt bei Säuglingen und Kleinkindern, die eine makrobiotische Ernährung erhalten, vor. Unter diesen Kindern entwickelten mehr als die Hälfte Symptome einer Rachitis.[3]
Ursachen
[Bearbeiten | Quelltext bearbeiten]Grundsätzlich wird die häufige Calcium-Mangel-Rachitis, die durch einen Vitamin-D-Mangel verursacht wird, von der seltenen Phosphat-Mangel-Rachitis unterschieden, bei der die Symptome durch einen vermehrten Verlust von Phosphat mit dem Urin durch die Nieren entstehen.
Calcium-Phosphat-Stoffwechsel
[Bearbeiten | Quelltext bearbeiten]Das Gleichgewicht des Calcium-Phosphat-Stoffwechsels ist durch die Hormone Parathormon, Calcitriol (Vitamin D) und Calcitonin in engen Grenzen geregelt. Die Konzentration der beiden Stoffe ist durch ein konstantes Löslichkeitsprodukt eng miteinander verknüpft. Der größte Teil des Vorrates an Calcium und Phosphat ist in Form von Hydroxylapatit in den Knochen gespeichert. Kommt es für eines der beiden Mineralien zu einem Ungleichgewicht zwischen Aufnahme über den Darm und Ausscheidung über die Nieren, werden Konzentrationschwankungen durch eine rasche Einlagerung in den Knochen oder Entspeicherung aus dem Knochen ausgeglichen. Vitamin D ist nicht nur für einen Einbau von Calcium und Phosphat in den Knochen (Mineralisation) nötig, sondern fördert zudem deren Aufnahme aus dem Darm und die Rückgewinnung aus dem Vorharn in den Nieren. Tritt ein Vitamin-D-Mangel ein, kann Calcium nur ungenügend aus dem Darm aufgenommen werden. Der hieraus resultierende Calciummangel führt zu einem unzureichenden Einbau von Hydroxylapatit in den wachsenden Knochen. Dieser wird zunehmend weicher und verformt sich. Gleichzeitig vermehrt sich die nicht verkalkte Knochengrundsubstanz (Osteoid), wodurch die Knochenauftreibungen im Bereich der Wachstumsfugen entstehen. Der Mensch stellt Vitamin D überwiegend aus einem Zwischenprodukt der Cholesterinbiosynthese, dem 7-Dehydrocholesterol, her. Dieses wird unter Einwirkung von Ultraviolettstrahlung aus dem Sonnenlicht in der Haut zu Vitamin D3 umgewandelt, in der Leber zu 25-Hydroxy-Cholecalciferol und anschließend in den Nieren durch die 1α-Hydroxylase zum eigentlich wirksamen Hormon 1,25-Dihydroxy-Cholecalciferol (Calcitriol) aktiviert. Nur ein kleiner Anteil des Vitamin-D-Bedarfs wird aus der Nahrung aufgenommen (genaueres siehe unter Vitamin D).
Calciummangel-Rachitis
[Bearbeiten | Quelltext bearbeiten]Bei der Calciummangel-Rachitis liegt ein Vitamin-D-Mangel vor. Die Ursachen des Vitamin-D-Mangels können in genetische, perinatale und kindliche Ursachen eingeteilt werden:[4]
- Genetische Ursachen sind Mutationen des Vitamin-D-Rezeptors, und Störungen der beiden Enzyme Cytochrom P450 2R1 (25-Hydroxylase) und 1α-Hydroxylase, die zur Synthese des aktiven Vitamin D notwendig sind. Dies führt zu einer Vitamin-D-Resistenz, d. h. die Rachitis bleibt trotz Gabe von Vitamin D bestehen.
- Prä- und perinatale Ursachen können Frühgeburtlichkeit, bereits bestehender mütterlicher Vitamin-D-Mangel und ausschließliches Stillen ohne Vitamin-D-Supplementation und ohne zeitgerechte Beikost sein.
- Kindliche Ursachen können Übergewicht, verminderte Sonnenexposition und Ernährungsprobleme sein. Diese können in einer Malabsorption bestehen, wenn nicht ausreichend Vitamin D und/oder Kalzium im Darm aufgenommen wird, wie bei Zöliakie oder Mukoviszidose, oder in einer Mangelernährung bestehen, wie bei Hungersituationen, vegetarischer bzw. veganer Diät oder multiplen Nahrungsmittel-Allergien, so dass die typischen Vitamin-D-Quellen Fisch, Eier, Milch fehlen.[5] Risikofaktoren für eine Mangelernährungs-bedingte Rachitis sind auch kürzliche Migration der Eltern und Entwicklungsstörungen des Kindes.
Sehr selten können auch bestimmte Medikamente zur Behandlung einer Epilepsie (Phenytoin, Phenobarbital) eine Rachitis durch verminderte Calcium-Aufnahme im Darm sowie gesteigerten Abbau des Vitamin D3 verursachen.
Phosphatmangel-Rachitis
[Bearbeiten | Quelltext bearbeiten]Eine Phosphatmangel-Rachitis wird zumeist durch einen vermehrten Verlust von Phosphat über die Nieren verursacht. Einzige Ausnahme stellen Frühgeborene dar, bei denen eine relativ auf das rasche Aufholwachstum bezogen unzureichende Phosphat-Zufuhr zugrunde liegen kann. Neben der erblich bedingten angeborenen familiären hypophosphatämischen Rachitis (Phosphatdiabetes) führen Schädigungen der Nierentubuli (De-Toni-Fanconi-Syndrom) – zumeist als Symptom einer angeborenen Cystinose, oder erworben durch Vergiftungen – zu einer phosphopenischen Rachitis.[5]
Es werden mehrere erbliche Formen der Phosphatmangel-Rachitis unterschieden. Die X-chromosomal dominant vererbte hypophosphatämische Rachitis ist die häufigste Form der vererbten Rachitis. Sie kommt rund einmal auf 20.000 Lebendgeborene vor. 70 % der Kranken weisen Mutationen des Phosphatregulatorgens PHEX auf dem X-Chromosom zustande. PHEX codiert für eine Protease, die kleine Peptidhormone spaltet. Die Protease wird in Zähnen, Knochen und den Nebenschilddrüsen exprimiert und führt über einen nicht geklärten Mechanismus zur Herunterregulation des Fibroblast-Growth-Factors 23 (FGF-23). Eine autosomal dominante Form der hypophosphatämischen Rachitis wird durch eine Mutation von FGF-23 verursacht. Außerdem ist auch eine erbliche Form mit erhöhter Kalziumausscheidung beschrieben.[6]
Symptome
[Bearbeiten | Quelltext bearbeiten]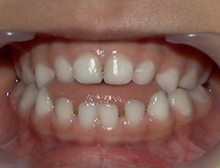


Im zweiten bis dritten Lebensmonat zeigen sich die ersten Symptome in Form von Unruhe, Schreckhaftigkeit, vermehrtem Schwitzen und dadurch ausgelöstem juckendem Hautausschlag (Miliaria). Etwa einen Monat später kommen eine Muskelschwäche mit Froschbauch, Verstopfungsneigung (Obstipation) und erste Knochenerweichungen am Schädel (Kraniotabes) hinzu. Jetzt kann der Calciummangel zusätzlich zu gesteigerter Muskelerregbarkeit (Tetanie) bis hin zu Krämpfen führen. Wiederum etwa einen Monat später entsteht durch Abflachung des Hinterkopfes und Auftreibung der Schädelnähte (Epiphytenbildung) das Bild eines Quadratschädels. Die perlschnurartig aufgereihten Auftreibungen der Knorpel-Knochen-Grenzen an den Wachstumsfugen der Rippen am Brustkorb wird auch Rosenkranz genannt. Auch Hand- und Fußgelenke verbreitern sich durch Auftreibung der Epiphysen zunehmend (Marfan-Zeichen, „doppelte Glieder“). Später zeigen sich ein verzögerter Zahndurchbruch, Defekte im Zahnschmelz, eine verzögerte Mineralisation der Kieferknochen bis hin zum offenen Biss. Weil der Brustkorb ungewöhnlich weich ist, führt der Muskelzug am Zwerchfellansatz zu einer Einziehung, der Harrison-Furche. Zu den weiteren typischen Knochenverformungen gehören Beinverkrümmungen (O-Beine, Genua vara), wobei die langen Röhrenknochen varisch (nach innen) verbogen sind, und die Fehlstellungen weniger im Gelenk selbst liegen. Bei Erwachsenen sind die Wachstumsfugen schon verschlossen und es kommt bei einem Vitamin-D-Mangel lediglich zu einer Osteomalazie ohne die im Kindesalter so typischen Knochenverformungen.
Diagnose
[Bearbeiten | Quelltext bearbeiten]
Die Diagnose wird durch die typischen Symptome, die im Röntgenbild sichtbaren Veränderungen an den Knochen sowie durch eine erhöhte Aktivität der Alkalischen Phosphatase im Blut gestellt.[5] Da die Röntgenuntersuchung keine spezifischen Unterscheidungsmerkmale zwischen einer Calciummangel- und einer Phosphatmangel-Rachitis zeigt, muss zwischen diesen Formen durch weitere Laboruntersuchungen unterschieden werden. Hierzu dient eine Bestimmung des Parathormons, das bei calcipenischer Rachitis erhöht und bei der phosphopenischen Form normal ist. Weiterhin wird die Konzentration der einzelnen Vitamin-D-Vorstufen bestimmt um eine klassische Vitamin-D-Mangel-Rachitis (mit erniedrigten 25(OH)Vitamin-D3-, aber niedrig normalen Dihydroxy-Cholecalciferol-Werten) von den Vitamin-D-abhängigen Formen (mit normaler 25(OH)Vitamin-D3- und abnorm niedriger Dihydroxy-Cholecalciferol-Konzentration bei der VDAR I beziehungsweise normaler Vitamin-D3- und exzessiv hoher Dihydroxy-Cholecalciferol-Konzentration bei der VDAR II) abzugrenzen.
Differentialdiagnose
[Bearbeiten | Quelltext bearbeiten]Abzugrenzen sind verschiedene Formen der Metaphysären Chrondrodysplasie, so z. B. Metaphysäre Chondrodysplasie Typ Jansen.
Therapie
[Bearbeiten | Quelltext bearbeiten]Die Behandlung richtet sich grundsätzlich nach der Ursache.

Bei der klassischen Vitamin-D-Mangel-Rachitis erfolgt die Therapie prinzipiell mit einer anfänglich hohen Gabe von Vitamin D und Kalzium, am besten auf täglicher Basis, um einer Hyperkalzämie vorzubeugen.[4]
Da es keine ausreichenden evidenz-basierten Empfehlungen gibt, hat 2016 ein internationales Expertengremium Konsens-Empfehlungen ausgearbeitet, unterschieden für Säuglinge unter drei Monaten, Säuglinge bis zu einem Jahr, Kinder unter zwölf Jahren und Kinder über zwölf Jahren.[8] Als tägliche Dosen haben Vitamin D2 (Ergocalciferol) und Vitamin D3 (Cholecalciferol) die gleiche Wirksamkeit.
Liegt eine schwere Hypokalzämie mit schweren Symptomen wie Epilepsie oder Tetanie vor, erfolgt die Kalziumgabe zunächst intravenös.
Wenn eine tägliche Gabe und Überwachung nicht möglich sind, kann auch eine hochdosierte Einzelgabe von Vitamin D erfolgen. Zur Kontrolle können die Serumspiegel von Kalzium, Phosphat, 25-Hydroxy-Vitamin-D, Parathormon und alkalischer Phosphatase, sowie die Kalzium-Kreatinin-Ratio im Urin in monatlichem Rhythmus bestimmt werden. Bei Mangelernährungs-bedingter Rachitis sind die Serumspiegel meist nach drei Monaten adäquater Therapie normalisiert, ebenso die Knochen im Röntgenbild, aber gelegentlich ist eine längere Therapie notwendig.
Wird bei einer schweren Rachitis Vitamin D gegeben, kann es zu einer anfänglichen paradoxalen Verschlechterung mit stärkerer Hypokalzämie kommen, da der demineralisierte Knochen dann Kalzium sehr schnell aufnehmen kann. Dies ist als hungry bone syndrom bekannt und bedarf teilweise sehr hoher Kalzium-Dosen.[4]
Nach abgeschlossener Behandlung ist eine dauerhafte Erhaltungstherapie bzw. Rezidiv-Prophylaxe mit Vitamin D und Kalzium notwendig.
Liegt jedoch eine Vitamin-D-abhängige Rachitis Typ I mit gestörter Umwandlung von Vitamin D3 in das aktive Dihydroxy-Cholecalciferol vor, muss neben einer hochdosierten Calcium-Substitution Calcitriol verabreicht werden. Sobald der weiche Knochen mit Calcium aufgesättigt ist, genügt eine lebenslange Substitution von Calcitriol. Die Vitamin-D-abhängige Rachitis Typ II wiederum gestaltet sich oft schwierig. Eine alleinige Calcium- und Dihydroxy-Cholecalciferol-Zufuhr in Form von Tabletten reicht hier unter Umständen nicht aus. In solchen Fällen sind zusätzliche Calcium-Infusionen nötig, um den Knochen entsprechend aufzusättigen. Anschließend muss Calcium weiterhin in extrem hohen Mengen eingenommen werden, um einen normalen Calcium-Spiegel im Blut aufrechtzuerhalten.[5]
Bei der phosphopenischen Form muss entsprechend neben einer Behandlung mit Calcitriol auch eine Substitution von Phosphat erfolgen (siehe Artikel Phosphatdiabetes).
Knochenfehlstellungen heilen bei Kindern bei der klassischen Rachitis nach Substitution von Vitamin D meist selbständig aus, bei schweren Verformungen der Beine werden allerdings oberschenkellange Schienen empfohlen (Orthesen). Bei den Phosphatmangel-Formen und bei Jugendlichen sind deutlich häufiger Korrekturosteotomien notwendig, bei denen durch eine Knochenkeilentnahme mit anschließender Osteosynthese der Achsfehler korrigiert wird.
Vorbeugung
[Bearbeiten | Quelltext bearbeiten]Entsprechend den Empfehlungen der Deutschen Gesellschaft für Sozialpädiatrie erhalten Säuglinge im ersten Lebensjahr von der zweiten Lebenswoche an eine vorbeugende Vitamin D3-Gabe, dort in Tablettenform. Die Ernährungskommission der Schweizerischen Gesellschaft für Pädiatrie sowie die Schweizerische Gesellschaft für Neonatologie empfehlen ab den ersten Lebenstagen eine tägliche Zufuhr von 300–500 I. E., die maximale Tagesdosis soll 1000 I. E. nicht überschreiten.[9] Verabreicht wird sie dort in einer Tropfenlösung.
Mit 300–600 I. E. (in Deutschland 500 I. E.) liegt die Dosierung deutlich über dem angenommen täglichen Bedarf von 100 bis 200 I. E., jedoch sollen damit natürliche Schwankungen genauso ausgeglichen werden wie gelegentlich vergessene Gaben. Diese Substitution wird für gestillte und flaschenernährte Säuglinge gleichermaßen während des gesamten ersten Lebensjahres und gegebenenfalls darüber hinaus durch den zweiten Lebenswinter hindurch empfohlen. Die vorgeschlagene Dosierung gilt auch bei zusätzlicher Anreicherung der industriell gefertigten Flaschenmilch mit Vitamin D als hinreichend sicher, da Überdosierungserscheinungen in Form von vermehrtem Durst, vermehrtem Wasserlassen, hartnäckiger Appetitlosigkeit, Verstopfung und Gedeihstörung in seltenen Fällen erst bei Dosierung über 2.000 I. E. beschrieben wurden.
Geschichte
[Bearbeiten | Quelltext bearbeiten]
Wie Knochenfunde und Untersuchungen von ägyptischen Mumien zeigen, hat es die Rachitis von der Vorgeschichte an zu allen Zeiten und in allen Teilen der Erde gegeben.[10] Die ersten Beschreibungen als eigenständiges Krankheitsbild stammen von Hieronymus Reusner aus dem 16. Jahrhundert. Bereits im 16. Jahrhundert wusste man die Krankheit durch Lebertran zu behandeln. Etwa hundert Jahre später wird der Name Morbus Anglorum („Englische Krankheit“[11]) von Whistler geprägt. Er sollte sich bis in das 19. Jahrhundert halten. Um 1620 wurde in den englischen Grafschaften Somerset und Dorset ein Auftreten der Krankheit beobachtet.[12] Im Jahr 1650[13] beschrieb Francis Glisson die Erkrankung erstmals[14] in allen Einzelheiten. Im 18. Jahrhundert häufen sich schließlich die Abhandlungen über die Rachitis.[10] In Europa trat die Rachitis nach den Weltkriegen bedingt durch Mangelernährung wieder verstärkt auf. Sie ist auch heute vorwiegend in den armen Ländern der Welt verbreitet. Die Grundlagen für die Behandlung dieser Krankheit wurden erst Anfang des 20. Jahrhunderts in England geschaffen. Der durch die Umweltverschmutzung durch die Industrie und private Holzfeuerung verursachte Smog legte sich damals bei bestimmten Wetterlagen häufig über Städte in Tal- und Kessellagen, so dass die UV-Strahlung der Sonne, die in der Haut die Reduktion von 7-Dehydrocholesterol zu Cholecalciferol bewirkt, teils abgeschirmt wurde. Die Folge war, dass viele Kinder die typischen Symptome zeigten. Interessanterweise traf die Krankheit auch die englische Oberschicht. Durch deren verglaste Wintergärten konnte ebenfalls nur wenig UV-Licht gelangen, wodurch Rachitis auch bei hohem Lebensstandard auftreten kann. Regelmäßige Lebertran-Gaben helfen, die Krankheit zu verhüten, da Lebertran besonders reich an Vitamin D ist. Ebenso ist viel Aufenthalt im Freien eine gute Vorbeugung. Der polnische Kinderarzt und Forscher, Jan Rudolf Raczyński (1865–1918),[15] der einen Zusammenhang der Rachitis auch mit einem Mangel an Sonnenlicht vermutete, schickte rachitische Kinder 1912 zur Heilung in die Karpaten.[16] Edward Mellanby und Elmer McCollum erzeugten durch speziell zubereitete Nahrung an Hunden und Ratten künstlich Rachitis, welche in allen Fällen durch Lebertran heilbar war. Dies führte zu der Annahme, dass Lebertran ein „antirachitisches Vitamin“ enthält.[17] Im Winter 1918/1919 heilte der deutsche Kinderarzt Kurt Huldschinsky junge Rachitis-Patienten vollständig durch UV-Bestrahlung[18] mit der künstlichen Höhensonne.[19] Seitdem tritt die Krankheit in Mitteleuropa nur noch selten auf.[20] Die Amerikaner Harry Steenbock und Alfred Fabian Heß (1875–1933) sowie L. F. Unger haben dann herausgefunden, dass in der Haut von Säugetieren ein Stoff (Provitamin) ist, der bei Bestrahlung zum antirachitischen Vitamin wird. Demzufolge wurden Nahrungsmittel, etwa Milch für Kinder, bestrahlt.[21][22]
Die autosomal-dominante Phosphatmangelrachitis wurde 1939 erstmals beschrieben.[6]
Rachitis bei Tieren
[Bearbeiten | Quelltext bearbeiten]Rachitis kommt bei in Gefangenschaft gehaltenen Tieren oder Haustieren vor allem bei wachsenden Vögeln, Reptilien und Amphibien vor. Auslösende Faktoren sind neben einem absoluten Calcium- oder Vitamin-D-Mangel und Kunstlicht ohne UV-Anteil häufig auch ein zu geringes Calcium:Phosphor-Verhältnis in der Nahrung. Dieses sollte etwa 1,5–2:1 betragen. Bei einer übermäßigen Phosphor-Aufnahme wird die Bildung von aktiviertem Vitamin D (1,25-Hydroxy-Vitamin D2 und D3) in den Nieren vermindert, sodass die Resorption von Calcium aus dem Darm vermindert ist.
Bei Vögeln kommt Rachitis vor allem bei Sing-, Papageien- und Hühnervögeln vor, die einseitig mit Körnermischungen aufgezogen werden. Das Calcium:Phosphor-Verhältnis vieler Samen ist sehr niedrig (Mais 1:17, Hirse und Sonnenblumenkerne etwa 1:6). Bei betroffenen Jungvögeln kommt es vor allem zur Verkrümmung des Brustbeins, des Oberschenkelknochens und des Tibiotarsus. Die Therapie erfolgt durch Futterumstellung und zusätzliche Gabe von Calcium und Vitamin D. Verkrümmte Knochen können nur noch durch eine Korrekturosteotomie und eine anschließende Osteosynthese korrigiert werden, in schweren Fällen muss der Vogel eingeschläfert werden.
Bei Reptilien sind ebenfalls ein ungenügendes Calcium:Phosphor-Verhältnis (hoher Anteil an Fleisch oder calciumarmen Insekten) sowie Vitamin-D-, Calcium- und/oder UV-Licht-Mangel die wichtigsten Rachitisursachen, aber auch ein Vitamin-D-Überschuss kann Auslöser sein. Bei Schildkröten wird vor allem der Rückenpanzer (Plastron) ungenügend mineralisiert, sodass dieser weich und verkrümmt (sattelförmig) erscheint. Bei Schlangen und Echsen kommt es vor allem zu Verkrümmungen der Wirbelsäule, wobei Knochenbrüche vor allem im Bereich der Lendenwirbelsäule („Buckelbildung“) auftreten können. Die „Rosenkranzbildung“ an den Rippen ist nur selten zur beobachten. Die Therapie erfolgt wie bei Vögeln. Prophylaktisch können 200 I. E./kg und Tag Vitamin D3, bei Fleischfütterung der Zusatz einer Vitamin-Mineralstoffmischung eingesetzt werden.
Bei Amphibien ist vor allem die einseitige Fütterung chitinreicher Insekten (Ca- und Vitamin-D-Mangel) Rachitis-auslösend. Typisch ist bei ihnen eine Verkürzung und Erweichung des Unterkiefers. Die Therapie erfolgt durch Futterumstellung und zusätzliche Gabe von Calcium und Vitamin D.
Bei Haussäugetieren ist Rachitis sehr selten. Bei Hunden lässt sich eine Rachitis zwar experimentell auslösen, kommt aber praktisch nie vor. Von einer Vitamin-D-Prophylaxe wie bei Kindern wird bei Hunden abgeraten, da es durch einen Calciumüberschuss zu Störungen der enchondralen Ossifikation kommt.
Literatur
[Bearbeiten | Quelltext bearbeiten]- K. Kruse: Aktuelle Aspekte der Vitamin-D-Mangel-Rachitis. In: Monatsschrift Kinderheilkunde, 6, 2000, 148, S. 588–595.
- M. J. Lentze u. a.: Pädiatrie – Grundlagen und Praxis. 2. Auflage. Springer 2002.
- K. Gabrisch, P. Zwart: Krankheiten der Heimtiere. 6. Auflage. Schlütersche, Hannover 2005, ISBN 3-89993-010-X.
- J. E. Scherberich: Kalzium-Phosphat- und Knochenstoffwechsel. In: Der Nephrologe, 3, 2008, S. 507–517.
- Irmtraut Sahmland: Rachitis (englische Krankheit, doppelte Glieder). In: Werner E. Gerabek, Bernhard D. Haage, Gundolf Keil, Wolfgang Wegner (Hrsg.): Enzyklopädie Medizingeschichte. De Gruyter, Berlin / New York 2005, ISBN 3-11-015714-4, S. 1211.
Weblinks
[Bearbeiten | Quelltext bearbeiten]Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ K. S. Scanlon (Hrsg.): Vitamin D expert panel meeting October 11-12, 2001, Atlanta, Ga. Final report. ( PDF; 391 kB; englisch) abgerufen am 20. April 2006.
- ↑ M. F. Holick: Resurrection of vitamin D deficiency and rickets. In: The Journal of Clinical Investigation, 2006, 116, S. 2062–2072, PMID 16886050, Volltext (englisch)
- ↑ P. C. Dagnelie, F. J. Vergote, W. A. van Staveren, H. van den Berg, P. G. Dingjan, J. G. Hautvast: High prevalence of rickets in infants on macrobiotic diets. In: Am J Clin Nutr. 51 (1990), S. 202–208. PMID 2154918
- ↑ a b c Yamini V. Virkud, Neil D. Fernandes, Ruth Lim, Deborah M. Mitchell, William T. Rothwell: Case 39-2020: A 29-Month-Old Boy with Seizure and Hypocalcemia. In: New England Journal of Medicine. Band 383, Nr. 25, 17. Dezember 2020, S. 2462–2470, DOI: 10.1056/NEJMcpc2027078 - Fallbeschreibung einer Mangelernährungs-bedingten Rachitis bei einem 29 Monate alten Jungen
- ↑ a b c d R. Schnabel, D. Haffner: Diagnostik und Therapie der Rachitis. In: Monatsschrift Kinderheilkunde. 2005, 153, S. 77–90.
- ↑ a b V. S. Jagtap, V. Sarathi, A. R. Lila, T. Bandgar, P. Menon, N. S. Shah: Hypophosphatemic rickets. In: Indian Journal of Endocrinology and Metabolism. Band 16, Nr. 2, 2012, S. 177–182. doi:10.4103/2230-8210.93733.
- ↑ Albert Gossauer: Struktur und Reaktivität der Biomoleküle. Verlag Helvetica Chimica Acta, Zürich 2006, ISBN 3-906390-29-2, S. 152.
- ↑ Craig F. Munns, Nick Shaw, Mairead Kiely, Bonny L. Specker, Tom D. Thacher, Keiichi Ozono, Toshimi Michigami, Dov Tiosano, M. Zulf Mughal, Outi Mäkitie, Lorna Ramos-Abad, Leanne Ward, Linda A. DiMeglio, Navoda Atapattu, Hamilton Cassinelli, Christian Braegger, John M. Pettifor, Anju Seth, Hafsatu Wasagu Idris, Vijayalakshmi Bhatia, Junfen Fu, Gail Goldberg, Lars Sävendahl, Rajesh Khadgawat, Pawel Pludowski, Jane Maddock, Elina Hyppönen, Abiola Oduwole, Emma Frew, Magda Aguiar, Ted Tulchinsky, Gary Butler, Wolfgang Högler: Global Consensus Recommendations on Prevention and Management of Nutritional Rickets. In: The Journal of Clinical Endocrinology and Metabolism. Band 101, Nr. 2, Februar 2016, S. 394–415, doi:10.1210/jc.2015-2175 - Internationale Konsensempfehlungen zur Behandlung
- ↑ Paediratica Vol. 22, No. 1, 2011, S. 7: Empfehlungen für die Ernährung gesunder Neugeborener in den ersten Lebenstagen (PDF) abgerufen am 17. April 2015
- ↑ a b J.-Ch. Sournia, J. Poulet, M. Martiny (Hrsg.): Illustrierte Geschichte der Medizin. Directmedia, Berlin 2004.
- ↑ J. F. L. Cappel: Versuch einer vollständigen Abhandlung über die sogenannte Englische Krankheit. Berlin u. a. 1787.
- ↑ Otto Westphal, Theodor Wieland, Heinrich Huebschmann: Lebensregler. Von Hormonen, Vitaminen, Fermenten und anderen Wirkstoffen. Societäts-Verlag, Frankfurt am Main 1941 (= Frankfurter Bücher. Forschung und Leben. Band 1), S. 52–54 (Die englische Krankheit), hier: S. 52.
- ↑ F. Glisson: De Rachitide sive Morbo puerili, qui vulgo the Rickets dicitur, tractatus. London 1650.
- ↑ Irmtraut Sahmland: Rachitis. 2005, S. 1210.
- ↑ Österreichisches Biographisches Lexikon: Raczyński, Jan Rudolf.
- ↑ Otto Westphal, Theodor Wieland, Heinrich Huebschmann: Lebensregler. Von Hormonen, Vitaminen, Fermenten und anderen Wirkstoffen. 1941, S. 52.
- ↑ Otto Westphal, Theodor Wieland, Heinrich Huebschmann: Lebensregler. Von Hormonen, Vitaminen, Fermenten und anderen Wirkstoffen. 1941, S. 52 f.
- ↑ Philipp Osten: Rachitis lässt sich durch ultraviolettes Licht heilen. In: Berliner Zeitung. 14. April 2007, archiviert vom (nicht mehr online verfügbar) am 24. September 2015; abgerufen am 19. Juni 2019. Info: Der Archivlink wurde automatisch eingesetzt und noch nicht geprüft. Bitte prüfe Original- und Archivlink gemäß Anleitung und entferne dann diesen Hinweis.
- ↑ Paul Diepgen, Heinz Goerke: Aschoff/Diepgen/Goerke: Kurze Übersichtstabelle zur Geschichte der Medizin. 7., neubearbeitete Auflage. Springer, Berlin/Göttingen/Heidelberg 1960, S. 60.
- ↑ Christian Floto: Sprechstunde; X-, O- oder ungleich lange Beine. Deutschlandfunk, 18. Juni 2019, abgerufen am 19. Juni 2019.
- ↑ Otto Westphal, Theodor Wieland, Heinrich Huebschmann: Lebensregler. Von Hormonen, Vitaminen, Fermenten und anderen Wirkstoffen. 1941, S. 53.
- ↑ Die Pirsch auf Rachitis.