Prostacyclin
| Strukturformel | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
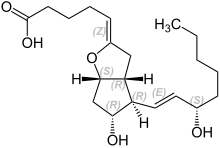
| |||||||||||||
| Allgemeines | |||||||||||||
| Freiname | Epoprostenol | ||||||||||||
| Andere Namen |
| ||||||||||||
| Summenformel | C20H32O5 | ||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||
| |||||||||||||
| Arzneistoffangaben | |||||||||||||
| ATC-Code | |||||||||||||
| Wirkstoffklasse | |||||||||||||
| Eigenschaften | |||||||||||||
| Molare Masse | 352,47 g·mol−1 | ||||||||||||
| Sicherheitshinweise | |||||||||||||
| |||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||
Prostacyclin (oder Synonym Prostaglandin I2, kurz PGI2) ist ein Eicosanoid und gehört zu der Gruppe der Serie-2-Prostaglandine, dies sind die entzündungsfördernden Prostaglandine aus der Arachidonsäure.
Geschichte
[Bearbeiten | Quelltext bearbeiten]Das Interesse am Einsatz von Prostaglandinen als Vasodilatatoren wurde bereits frühzeitig nach deren Entdeckung geweckt. Alprostadil (PGE 1) wurde erstmals mit guten Ergebnissen 1973 bei arteriosklerotischen Gefäßerkrankungen eingesetzt. Sechs Jahre später wurde Prostacyclin das erste Mal erfolgreich bei der Therapie für periphere arterielle Verschlusskrankheiten verwendet. Der große Nachteil dieser Substanzen allerdings war die deutliche Instabilität. Aus diesem Grund forschte man an Derivaten, die eine höhere Stabilität aufweisen. Daraufhin wurde das synthetische Iloprost[2] entwickelt, das eine deutlich höhere metabolische Stabilität besaß. Es wurde 1993 als Ilomedin auf den deutschen Markt gebracht.[3]
Bildung
[Bearbeiten | Quelltext bearbeiten]Prostacyclin wird in Endothelzellen mit Hilfe der Prostacyclinsynthase aus dem Prostaglandin PGH2 aus der Arachidonsäure gebildet.
Wirkungen
[Bearbeiten | Quelltext bearbeiten]Prostacyclin bindet an den IP-Rezeptor, einen G-Protein-gekoppelten Membranrezeptor, und entfaltet darüber unterschiedliche Wirkungen:
Entzündung
[Bearbeiten | Quelltext bearbeiten]PGI2 ist zusammen mit PGE2 das Hauptprostaglandin, welches in das Entzündungsgeschehen involviert ist. Es erhöht die Gefäßpermeabilität (was die Gewebeschwellung hervorruft), ist an der Entstehung der Rötung beteiligt (welche durch eine erhöhte Durchblutung zustande kommt) und verstärkt den Schmerz (welcher durch andere Entzündungsstoffe wie Bradykinin oder Histamin hervorgerufen wird), indem es nozizeptive Nervenendigungen sensibilisiert (indem es die Aktivierungsschwelle für Tetrodotoxin-resistente Natriumkanäle an sensiblen Nerven herabsetzt).[4] IP-Rezeptoren in sensiblen Neuronen erhöhen die Aktivität der Adenylylcyclase und der Phospholipase A und modulieren so die Aktivität der Ionenkanäle und der Neurotransmitterfreisetzung durch die Aktivierung von Proteinkinase A und der Proteinkinase C.
Kardiovaskuläres System
[Bearbeiten | Quelltext bearbeiten]Prostacyclin wirkt stark gefäßerweiternd (vasodilatierend) und thrombozytenaggregationshemmend.
- Gefäßzellen bilden viele Prostaglandine, Prostacyclin ist jedoch das Hauptprostaglandin, welches durch die Endothelzellen der Gefäße gebildet wird, in denen die Prostaglandin-I-Synthase angereichert vorkommt. Prostacyclin bindet an den G-Protein-gekoppelten Prostacyclin-Rezeptor der glatten Muskelzellen der Gefäße und hemmt über eine Erhöhung des intrazellulären cAMPs die Gefäßkontraktion. Es ist hier ein Gegenspieler des in Thrombozyten zumeist gebildeten Thromboxans.
- Ferner hemmt es den MAP-Kinase-Weg.
- Es hemmt die Thrombozytenaggregation und ist somit auch hier funktionell ein Gegenspieler des vor allem in den Thrombozyten gebildeten Thromboxans.
Prostacyclin bewirkt eine Reperfusion bzw. Verbesserung und Entstörung der Blutzirkulation.[5]
Endogenes Prostacyclin wird hauptsächlich im Gefäßendothel und der glatten Muskulatur gebildet. Es hat einen vasodilatativen, antiproliferativen und zytoprotektiven Effekt. Bei Prostacyclin handelt es sich um den am stärksten wirksamen endogenen Thrombozytenaggregationshemmer (TAH).
Die Thrombozytenaggregationshemmung kommt durch inhibitorische Wirkung auf Thrombozyten zustande. Prostacyclin wird zu 70 % renal eliminiert und wird hauptsächlich hepatisch metabolisiert.
Lunge
[Bearbeiten | Quelltext bearbeiten]Auch hier erweitert es vor allem die Lungengefäße und verhindert Mikrothromben. Ferner ist es ein schwacher Bronchodilatator. Die Prostacyclinblutspiegel von Patienten steigen unter Vollnarkose und Beatmung auf das 15–20-fache der Norm an.
Pharmakologie
[Bearbeiten | Quelltext bearbeiten]Therapeutische Anwendung
[Bearbeiten | Quelltext bearbeiten]Therapeutisch werden Prostacyclin (Epoprostenol) und Prostacyclinanaloga (Iloprost, Treprostinil) zur Behandlung des Raynaud-Syndroms, der Pulmonalen Hypertonie, im Off-Label-Use auch von Knochenmarködemen und der Femurkopfnekrose[6] eingesetzt.

Bei Patienten mit Heparin-induzierter Thrombozytopenie (HIT) kann Prostacyclin im Off-Label-Use eingesetzt werden, wenn z. B. für eine Herzoperation mit Herz-Lungen-Maschine Heparin gegeben werden muss. Prostacyclin als Dauerinfusion schützt dabei die Thrombozyten vor Aktivierung und Verklumpung solange Heparin im Blutkreislauf vorhanden ist.[7]
Das synthetische Iloprost ist ein stabiles Analogon des körpereigenen Prostacyclins. Es ist zugelassen zur Behandlung von akuten ischämischen Ereignissen aufgrund von peripheren arteriosklerotischen Verschlüssen oder diabetischer Angiopathien sowie zur Therapie der pulmonaren Hypertonie. Ferner findet es bei der Therapie der Sklerodermie und des Raynaud-Syndroms Anwendung.
Gegenanzeigen
[Bearbeiten | Quelltext bearbeiten]Ausschlusskriterien für die Behandlung sind Schwangerschaft, eine Behandlung mit Warfarin oder Heparin, Herzfehler, vorausgegangener Myokardinfarkt oder eine instabile Angina pectoris. Bei rückenmarksnahen Regionalanästhesie-Verfahren (Spinalanästhesie bzw. Periduralanästhesie) sollte Prostacyclin 30 Minuten vorher abgesetzt werden, kann aber sofort nach dem Eingriff wieder gegeben werden.[8][9]
Wechselwirkungen
[Bearbeiten | Quelltext bearbeiten]Bekannte Nebenwirkungen mit dem Wirkstoff Prostacyclin sind, insbesondere wegen der anfänglich auftretenden vasodilatatorischen Hypotonie, Kopfschmerzen, Flush (Gesichtsrötung), Schwitzen und Übelkeit, auch kardiale Nebenwirkungen wie Angina-pectoris-Symptomatik bis hin zu EKG-Veränderungen. Weiterhin können Agitation, Diarrhoe, Fieber, Parästhesien, Myalgien, Arrhythmie, Extrasystolen, Lungenembolie und Nierenschmerzen auftreten. Es können sehr häufig Nebenwirkungen wie Blutungen wie z. B. Epistaxis (Nasenbluten) oder Hämoptysis (blutiger Auswurf aus den Atemwegen), besonders dann, wenn zusätzlich auch andere gerinnungshemmende Arzneimittel (Antikoagulanzien) eingenommen werden, auftreten. Bei Patienten, die gleichzeitig auch mit anderen Thrombozytenaggregationshemmern oder Antikoagulanzien (Mitteln, die die Blutgerinnung aufhalten) behandelt werden, kann das Blutungsrisiko erhöht sein.
Weblinks
[Bearbeiten | Quelltext bearbeiten]Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ a b Externe Identifikatoren von bzw. Datenbank-Links zu Iloprost: CAS-Nr.: 78919-13-8, EG-Nr.: 636-055-8, ECHA-InfoCard: 100.163.887, PubChem: 5311181, ChemSpider: 4470703, DrugBank: DB01088, Wikidata: Q20817139. Andere Namen: (E)-5-{(3aS,4R,5R,6aS)-5-Hydroxy-4-[(E)-(3S,4RS)-3-hydroxy-4-methyloct-1-en-6-inyl]perhydropentalen-2-yliden}pentansäure; Ciloprost; ZK 36374 (Schering). Summenformel: C22H32O4. Molmasse: 360,49 g/mol.
- ↑ Wolf-Dieter Müller-Jahncke, Christoph Friedrich, Ulrich Meyer: Arzneimittelgeschichte. 2., überarb. und erw. Auflage. Wiss. Verl.-Ges, Stuttgart 2005, ISBN 978-3-8047-2113-5, S. 165.
- ↑ Simmons D et al. Cyclooxygenase Isoenzymes: The Biology of Prostaglandin Synthesis and Inhibition. Pharmacol Rev 2004;56:387–437.
- ↑ Thorsten Schmidt: Infusion, Hüftkopfanbohrung oder Infusion nach Hüftkopfanbohrung in der Behandlung der atraumatischen Femurkopfnekrose (FKN) und des Knochenmarködemsyndroms, Dissertation, Universität Regensburg 2009, S. 19 (PDF; 1,3 MB).
- ↑ Petje et al. Aseptische Knochennekrosen im Kindesalter. Orthopäde 10 (2002) 1027-1038. doi:10.1007/s00132-004-0634-3
- ↑ Heparin-induced thrombocytopenia and cardiac surgery. Abgerufen am 16. Dezember 2018.
- ↑ Wiebke Gogarten, Hugo Van Aken: Perioperative Thromboseprophylaxe - Thrombozytenaggregationshemmer - Bedeutung für die Anästhesie In: AINS - Anästhesiologie · Intensivmedizin · Notfallmedizin · Schmerztherapie. 47, 2012, S. 242–252, doi:10.1055/s-0032-1310414.
- ↑ S. A. Kozek-Langenecker, D. Fries, M. Gütl, N. Hofmann, P. Innerhofer, W. Kneifl, L. Neuner, P. Perger,T. Pernerstorfer, G. Pfanner, et al.: Lokoregionalanästhesien unter gerinnungshemmender Medikation. Empfehlungen der Arbeitsgruppe Perioperative Gerinnung (AGPG) der Österreichischen Gesellschaft für Anästhesiologie und Intensivmedizin (ÖGARI). DER ANAESTHESIST Volume 54, Number 5 (2005), 476-484, doi:10.1007/s00101-005-0827-0.