Picolinsäure
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|

| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Picolinsäure | ||||||||||||||||||
| Andere Namen |
Pyridin-2-carbonsäure | ||||||||||||||||||
| Summenformel | C6H5NO2 | ||||||||||||||||||
| Kurzbeschreibung |
farbloses, geruchloses kristallines Pulver[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 123,11 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Löslichkeit |
887 g·l−1 (20 °C)[1] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||||||||
Die Picolinsäure (Pyridin-2-carbonsäure) ist eine organische Verbindung, die zu den Heterocyclen (genauer: Heteroaromaten) zählt. Sie bestehen aus einem Pyridinring, der mit einer Carboxygruppe (–COOH) substituiert ist. Sie gehört mit den anderen beiden isomeren Nicotinsäure und Isonicotinsäure zur Stoffgruppe der Pyridincarbonsäuren mit der Summenformel C6H5NO2.
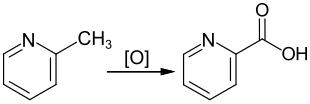
Darstellung
[Bearbeiten | Quelltext bearbeiten]Durch Oxidation, z. B. mittels Kaliumpermanganat (KMnO4), entsteht aus 2-Picolin die Picolinsäure.[2][3]
Verwandte Verbindungen
[Bearbeiten | Quelltext bearbeiten]Von der Picolinsäure leitet sich namentlich die Dipicolinsäure (Pyridin-2,6-dicarbonsäure) ab, die in unmittelbarer Nachbarschaft zum Stickstoffatom des Pyridins zwei Carboxygruppen trägt.
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c d e Eintrag zu Picolinsäure in der GESTIS-Stoffdatenbank des IFA, abgerufen am 2. Januar 2024. (JavaScript erforderlich)
- ↑ Shinkichi Shimizu, Nanao Watanabe, Toshiaki Kataoka, Takayuki Shoji, Nobuyuki Abe, Sinji Morishita, Hisao Ichimura: Pyridine and Pyridine Derivatives, in: Ullmann's Encyclopedia of Industrial Chemistry, 2002; doi:10.1002/14356007.a22_399.
- ↑ Harold Hart (Autor), Leslie E. Craine (Autor), David J. Hart (Autor), Christopher M. Hadad (Autor); Nicole Kindler (Übersetzer): Organische Chemie, 3. Auflage, Wiley-VCH, Weinheim 2007, ISBN 978-3-527-31801-8, S. 494.

