2,3-Dibrompropansäure
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|

| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | 2,3-Dibrompropansäure | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C3H4Br2O2 | ||||||||||||||||||
| Kurzbeschreibung |
hellgelber Feststoff[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 231,87 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest[1] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt | |||||||||||||||||||
| Löslichkeit |
sehr gut löslich in Benzol, Diethylether und Ethanol[2] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||||||||
2,3-Dibrompropansäure (Trivialname 2,3-Dibrompropionsäure) ist eine chemische Verbindung aus der Gruppe der aliphatischen Carbonsäuren mit drei Kohlenstoffatomen, bei denen zwei der an einem Kohlenstoffatom gebundenen Wasserstoffatome durch ein Bromatom ersetzt ist. Sie ist damit ein Derivat der Propionsäure.
Gewinnung und Darstellung
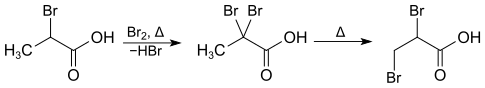
[Bearbeiten | Quelltext bearbeiten]2-Brompropionsäure kann durch Erhitzen mit elementarem Brom im geschlossenen Rohr in 2,2-Dibrompropansäure umgewandelt werden.[3], die sich beim weiteren Erhitzen in die 2,3-Dibrompropansäure umlagert.[4]
Ebenfalls möglich ist die Gewinnung durch Bromzugabe in Tetrachlorkohlenstoff-Medium zu Acrylsäure oder durch Hydrobromsäure-Hydrolyse von Methyl-2,3-dibrompropanoat gewonnen werden.[5][6]
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]2,3-Dibrompropansäure ist ein weißer bis hellgelber Feststoff[1], der sehr gut löslich in Benzol, Diethylether und Ethanol ist.[2]
Verwendung
[Bearbeiten | Quelltext bearbeiten]2,3-Dibrompropansäure kann als Ersatzstandard bei der Extraktion und Bestimmung von Halogenessigsäuren in Trinkwasser verwendet werden.[1] Sie kann auch zur Herstellung von Cyclopropancarbonsäuren[7] oder Vinyldihydrotetrazolon-Derivaten und Analoga zur Verwendung als NrF2-Aktivatoren verwendet werden.[8]
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c d e f g h Datenblatt 2,3-Dibrompropionsäure, 98% bei Sigma-Aldrich, abgerufen am 14. Mai 2022 (PDF).
- ↑ a b David R. Lide: CRC Handbook of Chemistry and Physics A Ready-reference Book of Chemical and Physical Data. CRC Press, 1995, ISBN 978-0-8493-0595-5, S. 160 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ O. Philippi, B. Tollens: "Untersuchungen über die Allylgruppe. XIII. Ueber die α-Bibrompropionsäure" in Justus Liebigs Annalen der Chemie, 1874, 171 (2), S. 313–333. doi:10.1002/jlac.18741710219.
- ↑ F. Beilstein: Handbuch der organischen Chemie, 3. Auflage, 1. Band. Verlag Leopold Voss, 1893. S. 480 (Volltext).
- ↑ Cristian Postolache, Lidia Matei: Synthesis of [α-T]polyacrylic acid. In: Journal of Labelled Compounds and Radiopharmaceuticals. Band 50, Nr. 5-6, 2007, S. 444–445, doi:10.1002/jlcr.1185.
- ↑ Comprehensive Organic Functional Group Transformations, Volume 5. Elsevier Science, 1995, ISBN 0-08-042326-4, S. 55 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Google Patents: CN104817453A - Novel method for synthesizing cyclopropanecarboxylic acid - Google Patents, abgerufen am 16. Mai 2022.
- ↑ Eintrag zu 2,3-Dibromopropanoic Acid bei Toronto Research Chemicals, abgerufen am 16. Mai 2022 (PDF).