Fettsäureamid-Hydrolase
| Fettsäureamid-Hydrolase | ||
|---|---|---|
| ||
| Masse/Länge Primärstruktur | 63066 Da, 579 Aminosäuren | |
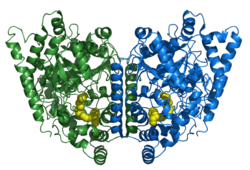
| Sekundär- bis Quartärstruktur | Homodimer | |
| Bezeichner | ||
| Externe IDs | ||
| Enzymklassifikationen | ||
| EC, Kategorie | 3.5.1.99, Hydrolase | |
| Reaktionsart | Hydrolyse | |
| Substrat | Anandamid + H2O | |
| Produkte | Arachidonsäure + Ethanolamin | |
| EC, Kategorie | 3.5.1.99, Hydrolase | |
| Reaktionsart | Hydrolyse | |
| Substrat | Oleamid + H2O | |
| Produkte | Ölsäure + NH3 | |
| Vorkommen | ||
| Homologie-Familie | Hovergen | |
| Orthologe | ||
| Mensch | Hausmaus | |
| Entrez | 2166 | 14073 |
| Ensembl | ENSG00000117480 | ENSMUSG00000034171 |
| UniProt | O00519 | O08914 |
| Refseq (mRNA) | NM_001441 | NM_010173.4 |
| Refseq (Protein) | NP_001432 | NP_034303.3 |
| Genlocus | Chr 1: 46.39 – 46.41 Mb | Chr 4: 115.99 – 116.02 Mb |
| PubMed-Suche | 2166 | 14073
|
Die Fettsäureamid-Hydrolase (FAAH, synonym: Oleamid-Hydrolase, Anandamid-Amidohydrolase) ist ein Enzym aus dem Fettstoffwechsel und ist am Endocannabinoid-System beteiligt.
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Die Fettsäureamid-Hydrolase ist eine Serin-Hydrolase und ein Transmembranprotein. Sie wurde erstmals 1993 als Anandamid-abbauendes Enzym beschrieben.[1] Die Fettsäureamid-Hydrolase hydrolysiert verschiedene Fettsäureamide. So wird beispielsweise Anandamid (N-Arachidonylethanolamin) 1 durch die Einwirkung von Wasser und FAAH in Arachidonsäure 2 und Ethanolamin gespalten:[2][3]

Die Hydrolysereaktion erfolgt als katalysierte Gleichgewichtsreaktion.[4] Auf dieselbe Weise können N-Acylethanolamine wie N-Oleoylethanolamin, N-Palmitoylethanolamin,[5] N-Acyl-Taurine[6] oder Ölsäureamid hydrolytisch gespalten werden. Die Hydrolyse von Ölsäureamid 3 führt beispielsweise zur Bildung von Ölsäure 4 und Ammoniak.[7]

FAAH hat eine Esterase- und eine Amidase-Enzymaktivität.[8] Sie wird verstärkt im Pankreas, im Gehirn, in der Niere, in der Skelettmuskulatur und der Plazenta gebildet. Im Gegensatz zu Ratten und Mäusen verfügt der menschliche Organismus nicht über die Isoform des Enzyms (FAAH2). Bei Stress wird die FAAH in der Amygdala aktiviert, wodurch die Konzentration an Anandamid gesenkt wird.[9] Daher ist die FAAH unter anderem an der Regulation von Angstzuständen beteiligt. Die Hemmung der FAAH wird als Behandlung für Angstzustände untersucht.[10] Weiterhin wird eine Hemmung der FAAH bei chronisch-entzündlichen Darmerkrankungen (IBD) und beim Reizdarmsyndrom (IBS) untersucht.[11] Die Hemmung der FAAH wird auch zur Behandlung von Tumorerkrankungen untersucht.[12]
Inhibitoren
[Bearbeiten | Quelltext bearbeiten]Es wurden verschiedene Inhibitoren für die Fettsäureamid-Hydrolase entwickelt,[13][14][15] z. B. URB597 (KDS-4103),[16] LY-2183240,[17] PF-622 und PF-750,[16] MK-4409,[18] und 4-Nonylphenylboronsäure.[19]
Der Wirkstoff BIA 10-2474 (von Bial-Portela & Ca. SA, Portugal) führte im Januar 2016 in einer klinischen Studie der Phase I zu unerwünschten Arzneimittelwirkungen, an denen ein Proband verstarb.[20] Diese Arzneimittelwirkung war zuvor bei anderen FAAH-Inhibitoren nicht beobachtet worden. So hat die Firma Pfizer 2012 die Entwicklung des FAAH-Inhibitors PF-04457845 wegen Wirkungslosigkeit in einer Phase-2-Studie abgebrochen.[21] Zuvor war es aber nicht zu negativen Reaktionen gekommen. Neben dieser publizierten Studie für die Indikation Schmerz, der durch Arthritis des Knies hervorgerufen wird, listet die Informationsseite des National Institutes of Health (NIH) im Januar 2016 drei weitere Studien mit PF-04457845, von denen eine beendet wurde, die beiden anderen aber noch Freiwillige rekrutieren. Indikationen sind das Tourette-Syndrom und die Behandlung von Cannabis-Entzug.[22] Weiterhin haben Vernalis und Sanofi FAAH-Inhibitoren entwickelt. Vernalis hat mit dem FAAH-Inhibitor V158866 eine Phase-1- sowie eine Phase-2-Studie abgeschlossen. Sanofi hat mit dem FAAH-Inhibitor SSR411298 eine Phase-2-Studie abgeschlossen und eine weitere abgebrochen. Auch Abbott Laboratories, Amgen und Renovis haben nicht-kovalente FAAH-Inhibitoren entwickelt.[23] Als aussichtsreicher selektiver FAAH-Inhibitor wird auch URB597 (KDS-4103) von Kandus Pharmaceuticals diskutiert.[24]
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ D. G. Deutsch, S. A. Chin: Enzymatic synthesis and degradation of anandamide, a cannabinoid receptor agonist. In: Biochemical pharmacology. Band 46, Nummer 5, September 1993, S. 791–796, PMID 8373432.
- ↑ B. F. Cravatt, K. Demarest, M. P. Patricelli, M. H. Bracey, D. K. Giang, B. R. Martin, A. H. Lichtman: Supersensitivity to anandamide and enhanced endogenous cannabinoid signaling in mice lacking fatty acid amide hydrolase. In: Proceedings of the National Academy of Sciences. Band 98, Nummer 16, Juli 2001, S. 9371–9376, doi:10.1073/pnas.161191698, PMID 11470906, PMC 55427 (freier Volltext).
- ↑ M. G. Cascio, P. Marini: Biosynthesis and Fate of Endocannabinoids. In: Handbook of experimental pharmacology. Band 231, 2015, S. 39–58, doi:10.1007/978-3-319-20825-1_2, PMID 26408157.
- ↑ D. Piomelli: More surprises lying ahead. The endocannabinoids keep us guessing. In: Neuropharmacology. Band 76 Pt B, Januar 2014, S. 228–234, doi:10.1016/j.neuropharm.2013.07.026, PMID 23954677, PMC 3855347 (freier Volltext).
- ↑ A. Saghatelian, S. A. Trauger, E. J. Want, E. G. Hawkins, G. Siuzdak, B. F. Cravatt: Assignment of endogenous substrates to enzymes by global metabolite profiling. In: Biochemistry. Band 43, Nummer 45, November 2004, S. 14332–14339, doi:10.1021/bi0480335, PMID 15533037.
- ↑ A. Saghatelian, M. K. McKinney, M. Bandell, A. Patapoutian, B. F. Cravatt: A FAAH-regulated class of N-acyl taurines that activates TRP ion channels. In: Biochemistry. Band 45, Nummer 30, August 2006, S. 9007–9015, doi:10.1021/bi0608008, PMID 16866345.
- ↑ B. F. Cravatt, O. Prospero-Garcia, G. Siuzdak, N. B. Gilula, S. J. Henriksen, D. L. Boger, R. A. Lerner: Chemical characterization of a family of brain lipids that induce sleep. In: Science. Band 268, Nummer 5216, Juni 1995, S. 1506–1509, PMID 7770779.
- ↑ M. P. Patricelli, B. F. Cravatt: Fatty acid amide hydrolase competitively degrades bioactive amides and esters through a nonconventional catalytic mechanism. In: Biochemistry. Band 38, Nummer 43, Oktober 1999, S. 14125–14130, PMID 10571985.
- ↑ O. Gunduz-Cinar, M. N. Hill, B. S. McEwen, A. Holmes: Amygdala FAAH and anandamide: mediating protection and recovery from stress. In: Trends in pharmacological sciences. Band 34, Nummer 11, November 2013, S. 637–644, doi:10.1016/j.tips.2013.08.008, PMID 24325918, PMC 4169112 (freier Volltext).
- ↑ C. J. Fowler: The potential of inhibitors of endocannabinoid metabolism as anxiolytic and antidepressive drugs–A practical view. In: European neuropsychopharmacology : the journal of the European College of Neuropsychopharmacology. Band 25, Nummer 6, Juni 2015, S. 749–762, doi:10.1016/j.euroneuro.2015.02.005, PMID 25791296.
- ↑ M. Sałaga, M. Sobczak, J. Fichna: Inhibition of fatty acid amide hydrolase (FAAH) as a novel therapeutic strategy in the treatment of pain and inflammatory diseases in the gastrointestinal tract. In: European journal of pharmaceutical sciences : official journal of the European Federation for Pharmaceutical Sciences. Band 52, Februar 2014, S. 173–179, doi:10.1016/j.ejps.2013.11.012, PMID 24275607.
- ↑ M. Nikan, S. M. Nabavi, A. Manayi: Ligands for cannabinoid receptors, promising anticancer agents. In: Life sciences. [elektronische Veröffentlichung vor dem Druck] Januar 2016, doi:10.1016/j.lfs.2015.12.053, PMID 26764235.
- ↑ Khanna IK, Alexander CW: Fatty acid amide hydrolase inhibitors--progress and potential. In: CNS Neurol Disord Drug Targets. 10. Jahrgang, Nr. 5, 2011, S. 545–58, doi:10.1517/17460441.2013.780021, PMID 21631410.
- ↑ Bisogno T, Maccarrone M: Latest advances in the discovery of fatty acid amide hydrolase inhibitors. In: Expert Opinion on Drug Discovery. 8. Jahrgang, Nr. 5, 2013, S. 509–22, doi:10.1517/17460441.2013.780021, PMID 23488865.
- ↑ J. L. Blankman, B. F. Cravatt: Chemical probes of endocannabinoid metabolism. In: Pharmacological reviews. Band 65, Nummer 2, April 2013, S. 849–871, doi:10.1124/pr.112.006387, PMID 23512546, PMC 3639726 (freier Volltext).
- ↑ a b Ahn K, Johnson DS, Fitzgerald LR, Liimatta M, Arendse A, Stevenson T, Lund ET, Nugent RA, Nomanbhoy TK, Alexander JP, Cravatt BF: Novel mechanistic class of fatty acid amide hydrolase inhibitors with remarkable selectivity. In: Biochemistry. 46. Jahrgang, Nr. 45, November 2007, S. 13019–30, doi:10.1021/bi701378g, PMID 17949010.
- ↑ Moore SA, Nomikos GG, Dickason-Chesterfield AK, Schober DA, Schaus JM, Ying BP, Xu YC, Phebus L, Simmons RM, Li D, Iyengar S, Felder CC: Identification of a High-Affinity Binding Site Involved in the Transport of Endocannabinoids. In: Proc. Natl. Acad. Sci. U.S.A. 102. Jahrgang, Nr. 49, Dezember 2005, S. 17852–7, doi:10.1073/pnas.0507470102, PMID 16314570, PMC 1295594 (freier Volltext).
- ↑ Chobanian HR, Guo Y, Liu P, Chioda MD, Fung S, Lanza TJ, Chang L, Bakshi RK, Dellureficio JP, Hong Q, McLaughlin M, Belyk KM, Krska SW, Makarewicz AK, Martel EJ, Leone JF, Frey L, Karanam B, Madeira M, Alvaro R, Shuman J, Salituro G, Terebetski JL, Jochnowitz N, Mistry S, McGowan E, Hajdu R, Rosenbach M, Abbadie C, Alexander JP, Shiao LL, Sullivan KM, Nargund RP, Wyvratt MJ, Lin LS, DeVita RJ: Discovery of MK-4409, a Novel Oxazole FAAH Inhibitor for the Treatment of Inflammatory and Neuropathic Pain. In: ACS Medicinal Chemistry Letters. 5. Jahrgang, Nr. 6, 2014, S. 717–21, doi:10.1021/ml5001239, PMID 24944750, PMC 4060928 (freier Volltext).
- ↑ Minkkilä A, Saario SM, Käsnänen H, Leppänen J, Poso A, Nevalainen T: Discovery of boronic acids as novel and potent inhibitors of fatty acid amide hydrolase. In: Journal of Medicinal Chemistry. 51. Jahrgang, Nr. 22, November 2008, S. 7057–60, doi:10.1021/jm801051t, PMID 18983140.
- ↑ Martin Enserink: More Details Emerge on Fateful French Drug Trial. In: Science. January 16, 2016 (sciencemag.org [ONLINE]).
- ↑ J. P. Huggins, T. S. Smart, S. Langman, L. Taylor, T. Young: An efficient randomised, placebo-controlled clinical trial with the irreversible fatty acid amide hydrolase-1 inhibitor PF-04457845, which modulates endocannabinoids but fails to induce effective analgesia in patients with pain due to osteoarthritis of the knee. Pain 153, Nr. 9, 2012, 1837–1846, PMID 22727500.
- ↑ clinicaltrials.gov
- ↑ J.M. Keith: Preclinical Characterization of the FAAH Inhibitor JNJ-42165279. In: ACS Medicinal Chemistry, Vol. 6, Nr. 12. 2015, S. 1204–1208.
- ↑ C. Grimaldi, A. Capasso: The Endocannabinoid System in the Cancer Therapy: An Overview. In: Current Medicinal Chemistry. 18. Jahrgang, Nr. 11, 2011, ISSN 0929-8673, S. 1575–1583, doi:10.2174/092986711795471374.