Methoxyphenole
| Methoxyphenole | ||||||||
| Name | 2-Methoxyphenol | 3-Methoxyphenol | 4-Methoxyphenol | |||||
| Andere Namen | o-Methoxyphenol, Brenzcatechin- monomethylether Guajacol |
m-Methoxyphenol, Resorcin- monomethylether |
p-Methoxyphenol, Hydrochinon- monomethylether MEHQ | |||||
| Strukturformel | 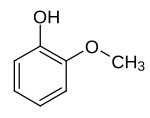
|

|
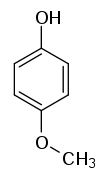
| |||||
| CAS-Nummer | 90-05-1 | 150-19-6 | 150-76-5 | |||||
| PubChem | 460 | 9007 | 9015 | |||||
| FL-Nummer | 04.005 | 04.076 | 04.077 | |||||
| Summenformel | C7H8O2 | |||||||
| Molare Masse | 124,14 g·mol−1 | |||||||
| Aggregatzustand | fest | flüssig | fest | |||||
| Schmelzpunkt | 28–32 °C[1] | −17,5 °C[1] | 56 °C[1] | |||||
| Siedepunkt | 205 °C[1] | 243–244 °C[1] | 243–244 °C[1] | |||||
| pKs-Wert[1] | 9,98 | 9,65 | 10,20 | |||||
| GHS- Kennzeichnung |
|
|
| |||||
| H- und P-Sätze | 302‐315‐319 | 302‐311‐315‐318‐332 | 302‐317‐319‐412 | |||||
| keine EUH-Sätze | keine EUH-Sätze | keine EUH-Sätze | ||||||
| 305+351+338 | 280‐305+351+338‐312 | 201‐273‐280‐308+313‐333+313‐337+313 | ||||||
Die Methoxyphenole (auch Hydroxyanisole) bilden eine Stoffgruppe, die sich sowohl vom Anisol als auch vom Phenol ableitet. Die Struktur besteht aus einem Benzolring mit angefügter Methoxy- (–OCH3) und Hydroxygruppe (–OH) als Substituenten. Durch deren unterschiedliche Anordnung (ortho, meta oder para) ergeben sich drei Konstitutionsisomere mit der Summenformel C7H8O2. In erster Linie kann man sie als methoxysubstituierte Phenole ansehen. Man kann sie auch als Monomethylether der Dihydroxybenzole (Brenzcatechin, Resorcin und Hydrochinon) auffassen. Das 2-Methoxyphenol ist unter seinem Trivialnamen Guajacol bekannt.
Vorkommen
[Bearbeiten | Quelltext bearbeiten]
Natürlich kommt 2-Methoxyphenol in Echtem Süßholz,[5] Holzteerkreosot und in Holzteeren sowie Guajakharz vor. 3-Methoxyphenol kann in Sesam nachgewiesen werden.[6] 4-Methoxyphenol wird in der Echten Bärentraube, Echtem Süßholz, der Gelben Schlauchpflanze und Sesam gefunden.[7]
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]4-Methoxyphenol hat aufgrund der größten Molekülsymmetrie den höchsten Schmelzpunkt. Die Methoxygruppe hat nur geringen Einfluss auf die Acidität der phenolischen OH-Gruppe, die pKs-Werte weisen nur geringfügige Unterschiede zum Phenol (9,99[1]) auf.
Darstellung
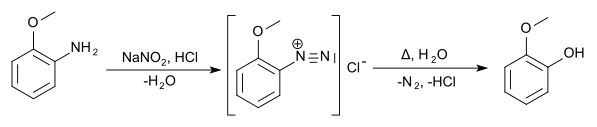
[Bearbeiten | Quelltext bearbeiten]Die Methoxyphenole sind aus den Anisidinen durch Verkochen ihrer Diazoniumsalze darstellbar.[8]
Sie können auch aus den Dihydroxybenzolen (Brenzcatechin, Resorcin und Hydrochinon) durch Veretherung mit Dimethylsulfat dargestellt werden.[9] Als Nebenprodukte bilden sich auch die Dimethoxybenzole.
Verwendung
[Bearbeiten | Quelltext bearbeiten]4-Methoxyphenol wird als Inhibitor zur Stabilisierung von monomeren Acrylaten verwendet. Man verwendet dafür auch die Abkürzung MEHQ.
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c d e f g h CRC Handbook of Tables for Organic Compound Identification, Third Edition, 1984, ISBN 0-8493-0303-6.
- ↑ Datenblatt Guaiacol bei Sigma-Aldrich, abgerufen am 3. Mai 2011 (PDF).
- ↑ Datenblatt 3-Methoxyphenol bei Sigma-Aldrich, abgerufen am 7. November 2016 (PDF).
- ↑ Datenblatt 4-Methoxyphenol bei Sigma-Aldrich, abgerufen am 22. September 2023 (PDF).
- ↑ O-METHOXY-PHENOL (englisch). In: Dr. Duke's Phytochemical and Ethnobotanical Database, Hrsg. U.S. Department of Agriculture, abgerufen am 24. Juli 2023.
- ↑ M-METHOXYPHENOL (englisch). In: Dr. Duke's Phytochemical and Ethnobotanical Database, Hrsg. U.S. Department of Agriculture, abgerufen am 24. Juli 2023.
- ↑ P-METHOXY-PHENOL (englisch). In: Dr. Duke's Phytochemical and Ethnobotanical Database, Hrsg. U.S. Department of Agriculture, abgerufen am 24. Juli 2023.
- ↑ Autorengemeinschaft: Organikum, 19. Auflage, Johann Ambrosius Barth, Leipzig · Berlin · Heidelberg 1993, ISBN 3-335-00343-8, S. 564.
- ↑ Autorengemeinschaft: Organikum, 19. Auflage, Johann Ambrosius Barth, Leipzig · Berlin · Heidelberg 1993, ISBN 3-335-00343-8, S. 209.