Prednicarbat
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
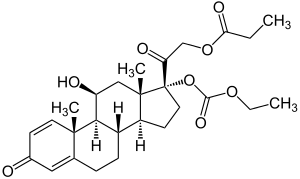
| ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Freiname | Prednicarbat | |||||||||||||||||||||
| Andere Namen | ||||||||||||||||||||||
| Summenformel | C27H36O8 | |||||||||||||||||||||
| Kurzbeschreibung |
weißes bis fastweißes, kristallines Pulver[1] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code | ||||||||||||||||||||||
| Wirkstoffklasse |
Glucocorticoid | |||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 488,6 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| Siedepunkt |
207–291 °C (Zersetzung)[4] | |||||||||||||||||||||
| Löslichkeit |
| |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Toxikologische Daten | ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||||||||
Prednicarbat ist ein Arzneistoff aus der Gruppe der topisch (örtlich) angewendeten Glucocorticoide, der zur Behandlung von verschiedenen Hautkrankheiten eingesetzt wird. Es handelt sich um ein mäßig stark wirksames Glucocorticoid („Klasse II“).[7]
Klinische Angaben
[Bearbeiten | Quelltext bearbeiten]Anwendungsgebiete (Indikationen)
[Bearbeiten | Quelltext bearbeiten]Prednicarbat wird angewendet bei akuten und chronischen entzündlichen Hauterkrankungen wie z. B. chronischem Ekzem. Bei Anwendung im Gesicht sollte darauf geachtet werden, dass das Medikament nicht in die Augen gelangt.[8] Die Anwendungskonzentration beträgt in der Regel 0,25 %.[9]
Art und Dauer der Anwendung
[Bearbeiten | Quelltext bearbeiten]Wie bei allen Corticoiden ist eine längerfristige Anwendung nach Möglichkeit zu vermeiden, da es sonst zu Hautatrophie, Teleangiektasien, Striae, einer speziellen Form der Akne, Perioraler Dermatitis und Hypertrichosis kommen kann. Es wird eine maximale Anwendungsdauer von 2 Wochen empfohlen.[8][10]
Gegenanzeigen (Kontraindikationen)
[Bearbeiten | Quelltext bearbeiten]Großflächige Anwendung von Corticoiden oder solche unter einem Okklusivverband sollten generell vermieden werden, um eine erhöhte Resorption des Wirkstoffs durch die Haut und somit die Gefahr systemischer, d. h. den gesamten Körper betreffender, unerwünschter Arzneimittelwirkungen zu verhindern.[9] Weitere Gegenanzeigen sind Überempfindlichkeit gegenüber dem Wirkstoff sowie die Anwendung am oder im Auge.[8]
Wechselwirkungen mit anderen Medikamenten
[Bearbeiten | Quelltext bearbeiten]Für Prednicarbat sind keine Wechselwirkungen bekannt.[8]
Anwendung während Schwangerschaft und Stillzeit
[Bearbeiten | Quelltext bearbeiten]Die großflächige Anwendung auf mehr als 30 % der Körperoberfläche ist nicht angezeigt, ebenso wie eine Anwendung im Brustbereich bei stillenden Müttern. Generell sollte während der Schwangerschaft die Indikation zur Anwendung von Prednicarbat streng gestellt und die Anwendung auf einen kleinen Hautbereich beschränkt werden.[8]
Besondere Patientengruppen (Diabetiker, Nierenkranke)
[Bearbeiten | Quelltext bearbeiten]Bei Säuglingen muss eine besonders sorgfältige Indikationsstellung erfolgen, da bei ihnen die Resorption des Wirkstoffes erhöht ist.[8]
Unerwünschte Wirkungen (Nebenwirkungen)
[Bearbeiten | Quelltext bearbeiten]Die Nebenwirkungen von Prednicarbat sind die gleichen wie bei anderen topischen Glucocorticoiden; siehe hierzu Glucocorticoide: Nebenwirkungen.
Pharmakologische Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Wirkungsmechanismus (Pharmakodynamik)
[Bearbeiten | Quelltext bearbeiten]Prednicarbat greift in den Arachidonsäurestoffwechsel ein, woraus eine Abnahme der Produktion von Entzündungsmediatoren wie z. B. Prostaglandinen oder Leukotrienen und damit eine antiinflammatorische Wirkung resultiert.
Auch eine antiallergische Wirkung ist vorhanden; diese beruht auf der Beeinflussung der Lymphozyten. Insbesondere wirkt die Substanz auf B- und T-Lymphozyten, deren Aktivität und Anzahl sich verringert.
Schließlich wirkt Prednicarbat noch antiproliferativ durch eine Verminderung der Stoffwechsel- und DNA-Syntheserate. Beides führt zu einer Verlangsamung der Zellteilung.[8] Diese Eigenschaft der Glucocorticoide erklärt ihre Wirksamkeit bei Psoriasis.
Aufnahme und Verteilung im Körper (Pharmakokinetik)
[Bearbeiten | Quelltext bearbeiten]Prednicarbat wird in der Haut zu Prednisolon-17-ethylcarbonat umgesetzt. Dieses weist eine wesentlich höhere Affinität zu entsprechenden Rezeptoren auf. Nach und nach zerfällt es zu Prednisolon. Ein Übertritt des Prednicarbats in den Blutkreislauf erfolgt bei korrekter Anwendung nicht.[8]
Toxikologie
[Bearbeiten | Quelltext bearbeiten]Prednicarbat hat sich im Tierversuch als „nicht hautreizend“ erwiesen, ebenso als weder phototoxisch noch photosensibilisierend.
Synthese
[Bearbeiten | Quelltext bearbeiten]Prednicarbat kann in einer dreistufigen Synthese hergestellt werden. Im ersten Schritt wird Prednisolon mit Tetraethylorthocarbonat zum Prednisolon-17,21-dieethylorthocarbonat umgesetzt. Eine saure Hydrolyse mittels Essigsäure ergibt unter Ringöffnung das Prednisolon-17-ethylcarbonat. Im letzten Schritt wird die Zielverbindung durch die Umsetzung mit Propionsäurechlorid in Gegenwart von Pyridin erhalten.[11]
Handelsnamen
[Bearbeiten | Quelltext bearbeiten]Prednitop, Dermatop
Siehe auch
[Bearbeiten | Quelltext bearbeiten]Glucocorticoide, Prednisolon, Hauterkrankung
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ Europäisches Arzneibuch, Deutscher Apotheker Verlag Stuttgart, 6. Ausgabe, 2008, S. -3738–3739, ISBN 978-3-7692-3962-1.
- ↑ G.W.A Milne: Ashgate Handbook of Endocrine Agents and Steroids. Routledge, 2017, ISBN 978-1-351-74347-1 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Datenblatt Prednicarbat bei Sigma-Aldrich, abgerufen am 16. Februar 2024 (PDF).
- ↑ a b H. Salvio Neto, Cs. Novák, J. R. Matos: Thermal analysis and compatibility studies of prednicarbate with excipients used in semi solid pharmaceutical form. In: Journal of Thermal Analysis and Calorimetry. Band 97, Nr. 1, 2009, S. 367, doi:10.1007/s10973-009-0234-x.
- ↑ a b c Cayman Chemical: Prednicarbate (73771-04-7), abgerufen am 21. Dezember 2019.
- ↑ a b Fagron: Sicherheitsdatenblatt Prednicarbat ( vom 21. Dezember 2019 im Internet Archive), abgerufen am 21. Dezember 2019.
- ↑ Glucorticoide topische In: Altmeyers Enzyklopädie Dermatologie online.
- ↑ a b c d e f g h Fachinformation Dermatop ( vom 13. Mai 2018 im Internet Archive), August 2017.
- ↑ a b Aktories, Förstermann, Hofmann, Starke: Allgemeine und spezielle Pharmakologie und Toxikologie, Urban & Schwarzenberg, München 2009, ISBN 978-3-437-42522-6.
- ↑ Rote Liste 2013.
- ↑ A. Kleemann, J. Engel, B. Kutscher, D. Reichert: Pharmaceutical Substances - Synthesis, Patents, Applications, 4. Auflage (2001) Thieme-Verlag Stuttgart, ISBN 978-1-58890-031-9.
