Tschitschibabin-Pyridin-Synthese
Die Tschitschibabin-Pyridin-Synthese ist eine Namensreaktion in der organischen Chemie und wurde erstmals im Jahre 1906 von dem russischen Chemiker Alexei Jewgenjewitsch Tschitschibabin veröffentlicht. Die Reaktion erlaubt die Synthese von Pyridin aus Aldehyden und Ammoniak.[1]
Übersichtsreaktion
[Bearbeiten | Quelltext bearbeiten]In einer cyclischen Kondensationsreaktion reagiert ein Aldehyd mit Ammoniak über einem Aluminiumkatalysators unter Wasserabspaltung zu einem Pyridin:[2][3]
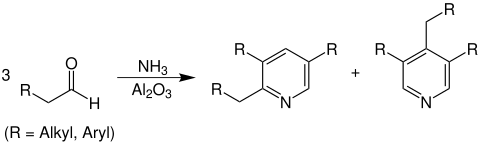
Reaktionsmechanismus
[Bearbeiten | Quelltext bearbeiten]Der Reaktionsmechanismus ist in der Literatur[3] beschrieben und wird am Beispiel von Acetaldehyd mit Ammoniak illustriert:

Acetaldehyd (1) reagiert mit Ammoniak (2) unter Abspaltung von Wasser und weiterem, durch Imin-Enamin-Isomerisierung (Imin-Enamin-Tautomerie) erzeugtem, Vinylamin zur Zwischenstufe 3. Wiederholte Reaktion mit Vinylamin (ein Enamin) liefert die Zwischenstufe 4. Anschließende Elektronenumlagerung mit Ladungsausgleich erzeugt einen Ringschluss unter Bildung der Zwischenstufe 5. Abspaltung von Ammoniak und Wasserstoff liefert das Pyridin-Derivat 6 (2-Picolin).
Anwendung
[Bearbeiten | Quelltext bearbeiten]Die Tschitschibabin-Pyridin-Synthese ist eine Schlüsselreaktion zur Synthese komplexer Pyridine. Benzaldehyd reagiert mit Acetophenon unter Zugabe von Ammoniumacetat und Essigsäure zu 2,4,6-Triphenylpyridin:[4]

Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ Chichibabin, A. E. J. In: Russ. Phys. Chem. Soc. 37, 1906, S. 1229.
- ↑ Tschitschibabin, A. E. and Oparina, M. P. (1927), Über die Kondensation des Crotonaldehyds mit Ammoniak bei Gegenwart von Aluminiumoxyd. Ber. dtsch. Chem. Ges. A/B, 60: 1877–1879, doi:10.1002/cber.19270600830 .
- ↑ a b Z. Wang: Comprehensive organic name reactions and reagents Volume 1. John Wiley, Hoboken (N.J.) 2009, ISBN 978-0-470-28662-3, S. 635–638.
- ↑ Marvin Weiss: Acetic Acid—Ammonium Acetate Reactions. An Improved Chichibabin Pyridine Synthesis In: J. Am. Chem. Soc. 74 (1), 1952, S. 200–202, doi:10.1021/ja01121a051.