Avibactam
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
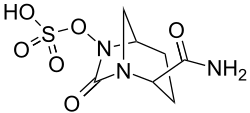
| ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Avibactam | |||||||||||||||
| Summenformel | C7H11N3O6S | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 265,24 g·mol−1 | |||||||||||||||
| Löslichkeit | ||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Avibactam ist ein Arzneistoff, der als Wirkverstärker für bestimmte Antibiotika eingesetzt wird, selbst aber keine antibiotische Wirkung hat. Es gehört zur Gruppe der β-Lactamase-Inhibitoren.
Wirkungsweise[Bearbeiten | Quelltext bearbeiten]
β-Lactamase-Inhibitoren hemmen das von den Bakterien gebildete Enzym β-Lactamase, mit dem die Bakterien bestimmte Antibiotika aus der Gruppe der Penicilline und Cephalosporine unwirksam machen. Die Produktion dieses Enzyms ist ein Mechanismus, durch den Bakterien resistent gegen diese Antibiotika sind oder werden können. Durch Hemmung dieses Enzyms kann dieser Resistenzmechanismus umgangen werden, indem die Zerstörung des Antibiotikums durch das bakterielle Enzym verhindert wird.[2]
Im Unterschied zu anderen β-Lactamase-Inhibitoren ist die kovalente Bindung an die β-Lactamase reversibel.
Anwendung[Bearbeiten | Quelltext bearbeiten]
In Kombination mit Ceftazidim[Bearbeiten | Quelltext bearbeiten]
Avibactam wurde im April 2016 - als Kombinationspräparat mit Ceftazidim; selbst hat es keine antibiotische Wirkung - für Europa zugelassen und wird von der Firma Pfizer unter dem Handelsnamen Zavicefta vertrieben. Laut Zulassung kann die Kombination Avibactam/Ceftazidim bei Erwachsenen und Kindern ab einem Alter von drei Monaten zur Behandlung der folgenden Infektionen angewendet:[3][4]
- komplizierte (schwer zu behandelnde) Infektionen von Geweben und Organen im Bauch (intraabdominalen Infektionen);
- komplizierte Infektionen in den Harnwegen, unter anderem Pyelonephritis (Nierenentzündung);
- nosokomiale Lungeninfektionen (im Krankenhaus erworbene Pneumonie), einschließlich beatmungsassoziierter Pneumonie (Lungenentzündung, die durch ein Beatmungsgerät entsteht, d. h. eine Maschine, die dem Patienten die Atmung erleichtert).
In Kombination mit Aztreonam[Bearbeiten | Quelltext bearbeiten]
Im März 2024 erhielt die fixe Kombination von Avibactam mit dem Monobactam Aztreonam (Handelsname: Emblaveo; Hersteller: Pfizer) vom Ausschuss für Humanarzneimittel (CHMP) der EMA die Zulassungsempfehlung zur Behandlung komplizierter Infektionen des Abdomens, der Harnwege, der krankenhauserworbenen Pneumonie sowie zur Behandlung von Infektionen durch aerobe gramnegative Organismen bei Erwachsenen mit begrenzten Behandlungsmöglichkeiten.[5] Pfizer hat Emblaveo gemeinsam mit Abbvie entwickelt.[6] Die Zulassung durch die Europäische Kommission ist nur noch Formsache.
Siehe auch[Bearbeiten | Quelltext bearbeiten]
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ a b c Cayman Chemical: Avibactam (sodium salt), abgerufen am 27. Dezember 2019.
- ↑ S. D. Lahiri, M. R. Johnstone u. a.: Avibactam and Class C β-Lactamases: Mechanism of Inhibition, Conservation of the Binding Pocket, and Implications for Resistance. In: Antimicrobial Agents and Chemotherapy. 58, 2014, S. 5704, doi:10.1128/AAC.03057-14.
- ↑ Zavicefta (Ceftazidim / Avibactam), EPAR der EMA - Übersicht, abgerufen am 23. März 2024
- ↑ Zusammenfassung der Merkmale des Arzneimittels, EPAR der EMA, abgerufen am 23. März 2024
- ↑ Emblaveo - European Medicines Agency. In: ema.europa.eu. 22. März 2024, abgerufen am 28. März 2024 (englisch).
- ↑ Pfizer Receives Positive CHMP Opinion for its Novel Antibiotic Combination for the Treatment of Patients with Multidrug-Resistant Infections and Limited Treatment Options, PM Pfizer vom 22. März 2024, abgerufen am 23. März 2024