Chelidamsäure
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|

| |||||||||||||||||||
| Tautomere Grenzstrukturen | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Chelidamsäure | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C7H5NO5 | ||||||||||||||||||
| Kurzbeschreibung |
weißer bis gelblicher Feststoff[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | |||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Chelidamsäure ist eine chemische Verbindung aus der Gruppe der Heterocyclen. Sie besteht aus einem Pyridinring mit Carboxygruppen in 2- und 6-Position und einer Hydroxygruppe in 4-Position.
Eigenschaften[Bearbeiten | Quelltext bearbeiten]
Chelidamsäure ist eine weiße bis schwach gelbliche Verbindung. Aus wässriger Lösung kristallisiert sie als Monohydrat aus. Chelidamsäuremonohydrat zersetzt sich bei 267 °C.[1] Chelidamsäure besitzt zwei tautomere Formen, eine aromatische Enolform und eine Ketoform. Das Monohydrat bildet im Kristall eine zwitterionische Struktur aus. In dieser ist eine Carbonsäuregruppe deprotoniert und der Stickstoff protoniert.[2]
Herstellung[Bearbeiten | Quelltext bearbeiten]
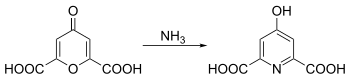
Chelidamsäure kann durch die Umsetzung von Chelidonsäure mit Ammoniak dargestellt werden.[3]
Verwendung[Bearbeiten | Quelltext bearbeiten]
Chelidamsäure kann als Ausgangsstoff zur Synthese heterocyclischer Verbindungen dienen. Die Hydroxygruppe kann leicht substituiert werden.[4] Die Carbonsäuregruppen können zum Aufbau größerer Strukturen genutzt werden.
Chelidamsäure bildet stabile Komplexe mit vielen Metallionen. Sie fungiert hierbei als dreizähniger Chelatligand.
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ a b c d e Datenblatt Chelidamic acid hydrate bei Sigma-Aldrich, abgerufen am 16. März 2011 (PDF).
- ↑ A. K. Hall, J. M. Harrowfield, B. W. Skelton, A. H. White: Chelidamic acid monohydrate: the proton complex of a multidentate ligand, in Acta. Cryst. 2000, C56, S. 448–450; doi:10.1107/S0108270199015620.
- ↑ L. Haitinger, A. Lieben: Untersuchungen über Chelidonsäure, in: Monatsh. Chem. 1885, 6, S. 279–328; doi:10.1007/BF01554631.
- ↑ M. K. Tse, S. Bhor, M. Klawonn, G. Anilkumar, H. Jiao, C. Döbler, A. Spannenberg, W. Mägerlein, H. Hugl, M. Beller: Ruthenium-Catalyzed Asymmetric Epoxidation of Olefins Using H2O2, Part I: Synthesis of New Chiral N,N,N-Tridentate Pybox and Pyboxazine Ligands and Their Ruthenium Complexes, in: Chemistry 2006, 12, S. 1855–1874; doi:10.1002/chem.200501261.
