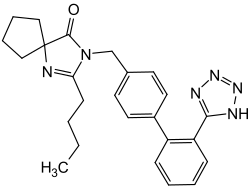
Irbesartan
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|

| ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Freiname | Irbesartan | |||||||||||||||||||||
| Andere Namen |
2-Butyl-3-({4-[2-(2H-1,2,3,4-tetrazol-5-yl)phenyl]phenyl}methyl)-1,3-diazaspiro[4.4]non-1-en-4-on (IUPAC) | |||||||||||||||||||||
| Summenformel | C25H28N6O | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code | ||||||||||||||||||||||
| Wirkstoffklasse | ||||||||||||||||||||||
| Wirkmechanismus | ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 428,54 g·mol−1 | |||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Irbesartan ist ein Arzneistoff aus der Gruppe der AT1-Antagonisten, der in der Behandlung von Bluthochdruck und leichter bis mittelschwerer Herzinsuffizienz, falls eine ACE-Hemmer-Therapie ungeeignet ist, eingesetzt wird.
Anwendungsgebiete (Indikationen)[Bearbeiten | Quelltext bearbeiten]
Irbesartan wird für die Behandlung folgender Krankheiten eingesetzt:[3]
- Essentielle Hypertonie
- Nierenerkrankung bei Patienten mit Hypertonie und Typ-2-Diabetes mellitus als Teil einer antihypertensiven Behandlung.
Darstellung und Gewinnung[Bearbeiten | Quelltext bearbeiten]
Die mehrstufige Synthese von Irbesartan geht vom Cyclopentanon aus, wobei im ersten Schritt durch die Umsetzung mit Natriumcyanid und Ammoniak das 1-Amino-1-cyclopentancarbonitril erhalten wird. Über eine Amidbildung mit Pentansäurechlorid und anschließende basische Zyklisierung wird eine Spirozwischenverbindung gebildet. Anschließend wird in Gegenwart von Natriumhydrid und Dimethylformamid mit 4′-(Brommethyl)-biphenyl-2-carbonitril die Biphenylsubstruktur in das Molekül eingefügt. Im letzten Syntheseschritt wird mittels Natriumazid durch Bildung der Tetrazolfunktion aus der Cyanogruppe die Zielverbindung erhalten.[4]
Eigenschaften[Bearbeiten | Quelltext bearbeiten]
Die Verbindung tritt in zwei polymorphen Kristallformen auf.[1]
-
Irbesartan, Polymorph A
-
Irbesartan, Polymorph B
Das Polymorph A schmilzt bei 181 °C mit einer Schmelzenthalpie von 91 J·g−1, Polymorph B bei 186 °C mit 116 J·g−1.[1] Beide Formen stehen monotrop zueinander. Das Polymorph B ist die thermodynamisch stabile Kristallform. Die beiden polymorphen Kristallformen unterscheiden sich hinsichtlich der Tautomerie der Tetrazolstruktur. Polymorph A entspricht der 4H-Tetrazolstruktur, Polymorph B der 2H-Tetrazolstruktur.[5][6] Das Polymorph A kristallisiert in einem hexagonalen Kristallsystem, das Polymorph B dagegen in einem triklinen Kristallsystem.[1]
Krebsgefährdende Verunreinigungen[Bearbeiten | Quelltext bearbeiten]
Aufgrund von Verunreinigungen mit dem potentiell krebserregenden N-Nitrosodiethylamin (NDEA) beim Wirkstoffhersteller Aurobindo Pharma Limited aus Hyderabad gab es seit Oktober 2018 mehrere Rückrufe Irbesartan-haltiger Medikamente.[7]
Handelsnamen[Bearbeiten | Quelltext bearbeiten]
Aprovel
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ a b c d e N. Boutonnet-Fagegaltier, J. Menegotto, A. Lamure, H. Duplaa, A. Caron, C. Lacabanne, M. Bauer: Molecular Mobility Study of Amorphous And Crystalline Phases of a Pharmaceutical Product by Thermally Stimulated Current Spectrometry. In: J Pharm Sci. Band 91, 2002, S. 1548–1560, doi:10.1002/jps.10146.
- ↑ a b Datenblatt Irbesartan, European Pharmacopoeia (EP) Reference Standard bei Sigma-Aldrich, abgerufen am 1. November 2016 (PDF).
- ↑ ROTE LISTE 2013. 53. Ausgabe. Verlag Rote Liste Service, Frankfurt am Main, ISBN 978-3-939192-70-1, S. 662.
- ↑ Axel Kleemann, Jürgen Engel, Bernd Kutscher, Dieter Reichert: Pharmaceutical Substances. 4. Auflage. 2 Bände. Thieme-Verlag, Stuttgart 2000, ISBN 1-58890-031-2; seit 2003 online mit halbjährlichen Ergänzungen und Aktualisierungen.
- ↑ M. Bauer, R. K. Harris, R. C. Rao, D. C. Apperley, C. A. Rodger: NMR study of desmotropy in irbesartan, a tetrazole-containing pharmaceutical compound. In: J. Chem. Soc. Perkin Trans. 1998, S. 475–481.
- ↑ Z. Böcskei, K. Simon, R. C. Rao, A. Caron, C. A. Rodger, M. Bauer: Irbesartan crystal form B. In: Acta Cryst. C 54, 1998, S. 808–810.
- ↑ NDEA: Zweiter Irbesartan-Rückruf, erstes Irbesartan-CEP zurückgezogen. In: Deutsche Apotheker Zeitung. 11. Oktober 2018.