1-Hexyl-3-methylimidazoliumtetrafluoroborat
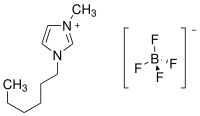
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | 1-Hexyl-3-methylimidazoliumtetrafluoroborat | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C10H19BF4N2 | ||||||||||||||||||
| Kurzbeschreibung |
hellorange Flüssigkeit[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 254,08 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
flüssig | ||||||||||||||||||
| Dichte |
1,149 g·cm−3[1] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
1-Hexyl-3-methylimidazoliumtetrafluoroborat ist ein organisches Salz, das als hellorange Flüssigkeit vorliegt. Auf Grund des geringen Schmelzpunkts ist es eine Raumtemperatur-ionische Flüssigkeit (RTIL).
Gewinnung und Darstellung[Bearbeiten | Quelltext bearbeiten]
1-Hexyl-3-methylimidazoliumtetrafluoroborat kann in einer Mikrowellenreaktion zwischen Ammoniumtetrafluoroborat und 1-Hexyl-3-methylimidazoliumchlorid oder 1-Hexyl-3-methylimidazoliumbromid gewonnen werden.[2] Alternativ kann auch 1-Hexylimidazol mit Trimethyloxoniumtetrafluoroborat zur Reaktion gebracht werden.[3]
Eigenschaften[Bearbeiten | Quelltext bearbeiten]
Das Salz hat mit −81 °C einen sehr niedrigen Schmelzpunkt.[1] Es besitzt eine elektrische Leitfähigkeit von 1,18 mS·cm−1 und ein elektrochemisches Fenster von 5,1 V.[4]
Verwendung[Bearbeiten | Quelltext bearbeiten]
Die Substanz wird als Komponente für Weltraum-Schmierstoffe untersucht.[5] Als Lösungsmittel kommt es in Cycloadditionen zum Einsatz, dabei können sowohl Mikrowellenstrahlung[6] als auch sonochemische Ansätze verfolgt werden.[7]
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ a b c d e f Datenblatt 1-Hexyl-3-methyl-imidazolium-tetrafluoroborat bei Sigma-Aldrich, abgerufen am 28. November 2021 (PDF).
- ↑ Vasudevan V Namboodiri, Rajender S Varma: An improved preparation of 1,3-dialkylimidazolium tetrafluoroborate ionic liquids using microwaves. In: Tetrahedron Letters. Band 43, Nr. 31, 2002, S. 5381–5383, doi:10.1016/S0040-4039(02)01075-4.
- ↑ Ruifeng Wang, Xiujuan Qi, Shimin Liu, Yude He, Youquan Deng: A comparison study on the properties of 1,3-dialkylimidazolium tetrafluoroborate salts prepared by halogen-free and traditional method. In: Journal of Molecular Liquids. Band 221, 2016, S. 339–345, doi:10.1016/j.molliq.2016.05.092.
- ↑ Iolitec: 1-Hexyl-3-methylimidazolium tetrafluoroborate. Abgerufen am 13. Februar 2021.
- ↑ Xiaoqiang Fan, Liping Wang: Highly Conductive Ionic Liquids toward High-Performance Space-Lubricating Greases. In: ACS Applied Materials & Interfaces. Band 6, Nr. 16, 2014, S. 14660–14671, doi:10.1021/am503941e.
- ↑ Ignacio López, Guadalupe Silvero, María José Arévalo, Reyes Babiano, Juan Carlos Palacios, José Luis Bravo: Enhanced Diels–Alder reactions: on the role of mineral catalysts and microwave irradiation in ionic liquids as recyclable media. In: Tetrahedron. Band 63, Nr. 13, 2007, S. 2901–2906, doi:10.1016/j.tet.2007.01.031.
- ↑ José Luis Bravo, Ignacio López, Pedro Cintas, Guadalupe Silvero, María José Arévalo: Sonochemical cycloadditions in ionic liquids. Lessons from model cases involving common dienes and carbonyl dienophiles. In: Ultrasonics Sonochemistry. Band 13, Nr. 5, 2006, S. 408–414, doi:10.1016/j.ultsonch.2005.07.001.
