4-Chlorbenzonitril
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
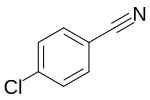
| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | 4-Chlorbenzonitril | ||||||||||||||||||
| Andere Namen |
p-Chlorbenzonitril | ||||||||||||||||||
| Summenformel | C7H4ClN | ||||||||||||||||||
| Kurzbeschreibung |
weißer bis gelblicher Feststoff mit bittermandelartigem Geruch[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 137,57 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest[1] | ||||||||||||||||||
| Dichte |
1,200 g·cm−3[2] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt |
223 °C[1] | ||||||||||||||||||
| Löslichkeit |
| ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
4-Chlorbenzonitril ist eine chemische Verbindung aus der Gruppe der Nitrile. Sie ist eine der drei isomeren Chlorbenzonitrile.
Gewinnung und Darstellung[Bearbeiten | Quelltext bearbeiten]
4-Chlorbenzonitril kann durch Reaktion von 4-Chlorbenzaldehydoxim[S 1] mit N-(p-Toluolsulfonyl)imidazol[S 2] gewonnen werden.[3]
Ebenfalls möglich ist die Synthese aus dem entsprechenden Aldehyd mit Ammoniak.[4]
Industriell wird die Verbindung durch Ammonoxidation von 4-Chlortoluol gewonnen.[5]
Eigenschaften[Bearbeiten | Quelltext bearbeiten]
4-Chlorbenzonitril ist ein brennbarer, schwer entzündbarer, kristalliner, weißer bis gelblicher Feststoff mit bittermandelartigem Geruch, der sehr schwer löslich in Wasser ist.[1]
Verwendung[Bearbeiten | Quelltext bearbeiten]
4-Chlorbenzonitril wird zur Herstellung von Amiden verwendet.[6] Es wird auch zur Herstellung eines roten Pigments für Kunststoffe und als Zwischenprodukt für Farbstoffe und pharmazeutische Wirkstoffe verwendet.[2]
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ a b c d e f g h Eintrag zu 4-Chlorbenzonitril in der GESTIS-Stoffdatenbank des IFA, abgerufen am 13. März 2022. (JavaScript erforderlich)
- ↑ a b c Datenblatt 4-Chlorobenzonitrile, 99% bei Alfa Aesar, abgerufen am 13. März 2022 (Seite nicht mehr abrufbar).
- ↑ Mohammad Navid Soltani Rad, Ali Khalafi-Nezhad, Somayeh Behrouz, Zohreh Amini, Marzieh Behrouz: Simple and Highly Efficient Procedure for Conversion of Aldoximes to Nitriles Using N-(p-Toluenesulfonyl) Imidazole. In: Synthetic Communications. Band 40, Nr. 16, 2010, S. 2429–2440, doi:10.1080/00397910903261395.
- ↑ Akira Misono, Tetsuo Osa, Seiichiro Koda: The Synthesis of Nitriles From Aldehydes. In: Bulletin of the Chemical Society of Japan. Band 39, Nr. 4, 1966, S. 854–854, doi:10.1246/bcsj.39.854.
- ↑ Peter Pollak, Gérard Romeder, Ferdinand Hagedorn, Heinz-Peter Gelbke: Nitriles - Ullmann's Encyclopedia of Industrial Chemistry. Wiley-VCH Verlag & Co. KGaA, Weinheim, Germany 2000, doi:10.1002/14356007.a17_363.
- ↑ Datenblatt 4-Chlor-benzonitril, 99% bei Sigma-Aldrich, abgerufen am 13. März 2022 (PDF).
Anmerkungen[Bearbeiten | Quelltext bearbeiten]
- ↑ Externe Identifikatoren von bzw. Datenbank-Links zu 4-Chlorbenzaldehydoxim: CAS-Nummer: 3848-36-0, PubChem: 5356407, Wikidata: Q82227883.
- ↑ Externe Identifikatoren von bzw. Datenbank-Links zu N-Tosylimidazol: CAS-Nummer: 2232-08-8, EG-Nummer: 218-771-9, ECHA-InfoCard: 100.017.066, PubChem: 75219, Wikidata: Q72495292.
