Benzylisothiocyanat
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
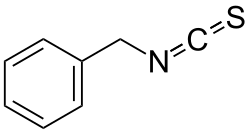
| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Benzylisothiocyanat | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C8H7NS | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 149,21 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
flüssig[1] | ||||||||||||||||||
| Dichte |
1,125 g·cm−3 (25 °C)[1] | ||||||||||||||||||
| Siedepunkt |
242–243 °C[1] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Benzylisothiocyanat (IUPAC) ist eine aromatische organische Verbindung aus der Gruppe der Isothiocyanate.
Vorkommen[Bearbeiten | Quelltext bearbeiten]

Benzylisothiocyanat kann aus Pflanzen verschiedener Familien extrahiert werden, unter anderem Cruciferae, Moringaceae und Caricaceae.[2] Es wurde beispielsweise in Papayas nachgewiesen, wo es vor allem in den Kernen vorkommt,[2][3] und im Zahnbürstenbaum.[4] Außerdem kommt es im Braunen Senf[5], Blumenkohl und Rettich[6], in Knoblauchsrauke[7], Gartenkresse[8] und der Großen Kapuzinerkresse[9] vor. Die Verbindung liegt als Benzylglucosinolat vor und wird bei Verletzung von Gewebe durch das Enzym Myrosinase daraus freigesetzt.[10] In geringen Mengen wird es auch von intakten Früchten abgesondert.[2]
Eigenschaften[Bearbeiten | Quelltext bearbeiten]
Benzylisothiocyanat ist für den scharfen Geschmack von Papayakernen verantwortlich.[11] Die Verbindung ist antimikrobiell und fungizid.[2][4] Daneben wirkt es auch als Anthelmintikum.[3]
Verwendung[Bearbeiten | Quelltext bearbeiten]
Benzylisothiocyanat ist in der EU unter der FL-Nummer 12.102 als Aromastoff für Lebensmittel allgemein zugelassen.[12]
Die Wirkung von Papayasamen, die traditionell als Antiparasitikum verwendet werden (z. B. in Indien), geht auf Benzylisothiocyanat zurück.[3]
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ a b c d e Datenblatt Benzylisothiocyanat bei Sigma-Aldrich, abgerufen am 13. Mai 2023 (PDF).
- ↑ a b c d Chung-Shih Tang: Benzyl isothiocyanate of papaya fruit. In: Phytochemistry. Band 10, Nr. 1, Januar 1971, S. 117–121, doi:10.1016/S0031-9422(00)90258-9.
- ↑ a b c Rohan Kermanshai, Brian E McCarry, Jack Rosenfeld, Peter S Summers, Elizabeth A Weretilnyk, George J Sorger: Benzyl isothiocyanate is the chief or sole anthelmintic in papaya seed extracts. In: Phytochemistry. Band 57, Nr. 3, Juni 2001, S. 427–435, doi:10.1016/S0031-9422(01)00077-2.
- ↑ a b Abier Sofrata, Ellen M. Santangelo, Muhammad Azeem, Anna-Karin Borg-Karlson, Anders Gustafsson, Katrin Pütsep: Benzyl Isothiocyanate, a Major Component from the Roots of Salvadora Persica Is Highly Active against Gram-Negative Bacteria. In: PLoS ONE. Band 6, Nr. 8, 1. August 2011, S. e23045, doi:10.1371/journal.pone.0023045, PMID 21829688, PMC 3148225 (freier Volltext).
- ↑ Zi-Tao Jiang, Rong Li, Yu-Min Zuo: Composition of Essential Oil of Brassica juncea (L.) Coss. from China. In: Journal of Essential Oil Research. Band 11, Nr. 4, Juli 1999, S. 503–506, doi:10.1080/10412905.1999.9701196.
- ↑ Mardey Liceth Cuellar-Nuñez, Ivan Luzardo-Ocampo, Sarah Lee-Martínez, Michelle Larrauri-Rodríguez, Guadalupe Zaldívar-Lelo de Larrea, Rosa Martha Pérez-Serrano, Nicolás Camacho-Calderón: Isothiocyanate-Rich Extracts from Cauliflower (Brassica oleracea Var. Botrytis) and Radish (Raphanus sativus) Inhibited Metabolic Activity and Induced ROS in Selected Human HCT116 and HT-29 Colorectal Cancer Cells. In: International Journal of Environmental Research and Public Health. Band 19, Nr. 22, 13. November 2022, S. 14919, doi:10.3390/ijerph192214919, PMID 36429638, PMC 9691161 (freier Volltext).
- ↑ Blažević, Ivica, and Josip Mastelić. "Free and bound volatiles of garlic mustard (Alliaria petiolata)." Croatica chemica acta 81.4 (2008): 607–613.
- ↑ Fekadu Kassie, Brenda Laky, Richard Gminski, Volker Mersch-Sundermann, Gerlinde Scharf, Evelyn Lhoste, Siegfried Kansmüller: Effects of garden and water cress juices and their constituents, benzyl and phenethyl isothiocyanates, towards benzo(a)pyrene-induced DNA damage: a model study with the single cell gel electrophoresis/Hep G2 assay. In: Chemico-Biological Interactions. Band 142, Nr. 3, Januar 2003, S. 285–296, doi:10.1016/S0009-2797(02)00123-0.
- ↑ Ana Pintão, M. Pais, Helen Coley, Lloyd Kelland, Ian Judson: In Vitro and In Vivo Antitumor Activity of Benzyl Isothiocyanate: A Natural Product from Tropaeolum majus. In: Planta Medica. Band 61, Nr. 03, Juni 1995, S. 233–236, doi:10.1055/s-2006-958062.
- ↑ Ze-You Li, Yong Wang, Wen-Tao Shen, Peng Zhou: Content determination of benzyl glucosinolate and anti–cancer activity of its hydrolysis product in Carica papaya L. In: Asian Pacific Journal of Tropical Medicine. Band 5, Nr. 3, 1. März 2012, S. 231–233, doi:10.1016/S1995-7645(12)60030-3.
- ↑ Seok Shin Tan: Papaya (Carica papaya L.) Seed Oil. In: Fruit Oils: Chemistry and Functionality. Springer International Publishing, Cham 2019, ISBN 978-3-03012472-4, S. 615–626, doi:10.1007/978-3-030-12473-1_31.
- ↑ Food and Feed Information Portal Database | FIP. Abgerufen am 15. Oktober 2023.

