Brivudin
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
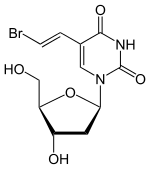
| ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Freiname | Brivudin | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C11H13BrN2O5 | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||
| ATC-Code | ||||||||||||||||
| Wirkstoffklasse |
Nukleosidanaloga | |||||||||||||||
| Wirkmechanismus |
Hemmung der viralen DNA-Polymerase | |||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 333,135 g·mol−1 | |||||||||||||||
| Schmelzpunkt |
164–166 °C[1] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Brivudin ist ein Arzneistoff, der als Virostatikum gegen Herpes simplex Typ 1 und Herpes Zoster eingesetzt werden kann. Es gehört zur Gruppe der Nukleosidanaloga. Im Vergleich zu anderen Nukleosidanaloga (Aciclovir, Valaciclovir, Famciclovir) zeichnet es sich durch eine wesentlich (200- bis 1000-fach) höhere antivirale Potenz aus und durch eine lange Halbwertszeit sowie intrazelluläre Verweildauer. Die häufigste Nebenwirkung ist Übelkeit, insgesamt sind Nebenwirkungen aber selten.
Geschichte[Bearbeiten | Quelltext bearbeiten]
Brivudin wurde schon in den 1970er Jahren in England und der damaligen DDR hergestellt. Aber erst seit einer Indikationsänderung im Jahr 2001 findet es breitere Verwendung. Bis zum Jahr 2000 war es zur Therapie von Herpes-simplex-Infektionen zugelassen. Seit 2001 wird es zur Behandlung von Herpes zoster angewendet.
Pharmakologie[Bearbeiten | Quelltext bearbeiten]
Wirkmechanismus[Bearbeiten | Quelltext bearbeiten]
Brivudin ist ein Thymidin-Antimetabolit, es wirkt gegen DNA-Viren.
In mehreren Phosphorylierungsschritten wird Brivudin zum Triphosphat aktiviert. Die Aktivierung erfolgt nur in der virusinfizierten Zelle, weil der Vorgang durch eine virale Thymidinkinase katalysiert wird. Die Triphosphate stellen die eigentliche Wirkform dar. Sie führen zur Hemmung der viralen DNA-Polymerase, zum Einbau von veränderten Nukleinbasen in die DNA und folglich zum Kettenabbruch während der DNA-Elongation.
Brivudin-Triphosphat hat eine sehr lange intrazelluläre Verweildauer von 10 Stunden, so dass es auch genug Zeit hat, um seine Wirkung in der von Viren befallenen Zellen zu entfalten. Da Brivudin nur die Virusreplikation hemmt, aber nicht das Virus selbst schädigt, kann es nur den Infektionsablauf unterdrücken. Es kann aber keine Erregereradikation bewirken und die für Herpesviren typischen Rezidive nicht verhindern.
Wirkspektrum[Bearbeiten | Quelltext bearbeiten]
Brivudin hat eine hohe Aktivität gegen Herpesviren. Es ist wirksam gegen Herpes simplex Typ 1 und gegen Varicella-Zoster-Viren. Dagegen ist es gegen Herpes simplex Typ 2 (z. B. genitale Infektionen) kaum wirksam. In vitro ist Brivudin auch gegen das Epstein-Barr-Virus wirksam. Eine Fallstudie zur Behandlung einer EBV-Enzephalitis bestätigte die Wirksamkeit auch in vivo.[3]
Wirksamkeit[Bearbeiten | Quelltext bearbeiten]
Brivudin ist wesentlich stärker gegen Herpesviren wirksam als andere Nukleosidanaloga (z. B. Aciclovir). Als Kriterium wird die Zeit vom Beginn der Behandlung bis zum letztmaligen Auftreten neuer Bläschen herangezogen. Bei Aciclovir beträgt diese Zeitspanne 18 Stunden, bei Brivudin 13 bis 14 Stunden.
Darüber hinaus tritt die postzosterische Neuralgie nach einer Behandlung mit Brivudin signifikant seltener auf als nach einer Behandlung mit Aciclovir.[4] Gegenüber Famciclovir zeigt sich kein Unterschied.
Die signifikant bessere Wirksamkeit von Brivudin gegenüber Aciclovir ist umstritten. Das arznei-telegramm verweist auf mögliche Interessenskonflikte der Verfasser der Brivudin-favorisierenden AWMF-Leitlinie und bezweifelt die klinische Relevanz der maßgeblichen Studien.[5]
Bei der Behandlung von Herpes corneae ist Brivudin gegenüber Idoxuridin signifikant überlegen.[6]
Indikationen und Dosierung[Bearbeiten | Quelltext bearbeiten]
Brivudin ist indiziert bei Herpes zoster und Herpes simplex Typ 1. Insbesondere bei Patienten über 50 Jahren ist es für diese Indikation das Mittel der Wahl.
Es wird oral angewendet. Die Standarddosierung beim Erwachsenen beträgt 125 mg pro Tag über 7 Tage. Die Tablette soll jeden Tag ungefähr zum gleichen Zeitpunkt eingenommen werden. Bei Patienten mit Nieren- oder Leberinsuffizienz ist keine Dosisanpassung nötig.[7]
Wichtig für den Behandlungserfolg ist, dass die Therapie möglichst innerhalb von 72 Stunden nach dem Beginn der Hautsymptomatik erfolgt (= Phase der Virusreplikation). Ein späterer Behandlungsbeginn ist noch sinnvoll, solange noch frische Bläschen vorhanden sind, wenn sich Anzeichen einer viszeralen Ausbreitung zeigen oder bei floridem Zoster ophthalmicus und Zoster oticus.
Nebenwirkungen[Bearbeiten | Quelltext bearbeiten]
Brivudin wird meistens gut vertragen. Die häufigsten Nebenwirkungen betreffen den Gastrointestinaltrakt: bei 2 % der Patienten kommt es zu Übelkeit. Auch eine Diarrhoe (Durchfall) kann auftreten.
Seltene Nebenwirkungen sind:
- Störungen des Nervensystems: Kopfschmerzen, Schwindel etc.,
- Müdigkeit oder Schlafstörungen,
- Anstieg von Serum-Kreatinin und -harnstoff (Hinweise auf Einschränkung der Nierenfunktion),
- Überempfindlichkeitsreaktionen der Haut,
- Blutbildveränderungen (reversibel).
Wechselwirkungen und Anwendungsbeschränkungen[Bearbeiten | Quelltext bearbeiten]

- Brivudin darf nicht gleichzeitig oder zeitnah mit dem Zytostatikum 5-Fluoruracil oder anderen 5-Fluorpyrimidinen (z. B. Tegafur) verabreicht werden. Mindestens 4 Wochen müssen zwischen der Gabe dieser Medikamente liegen, da der Metabolit des Brivudins, Bromvinyluracil, irreversibel das Enzym Dihydropyrimidindehydrogenase hemmt, das für den Abbau von Pyrimidinen zuständig ist. Das führt zu einer Kumulation und erhöhten Toxizität von 5-Fluoruracil, verbunden mit der Gefahr schwerer Nebenwirkungen: erhebliche gastrointestinale Störungen, Neutropenie und Knochenmarksdepression. Bei der gleichzeitigen Gabe von 5-Fluoruracil und Sorivudin, welches so wie Brivudin zum Metaboliten Bromvinyluracil abgebaut wird, hat diese Interaktion sogar zu Todesfällen geführt.[8] Diese potenziell tödliche Wechselwirkung mit antineoplastisch (5-Fluorouracil, Capecitabin, Floxuridin, Tegafur) oder antimykotisch wirksamen 5-Fluoropyrimidinen (5-Fluorcytosin) ist prinzipiell auch für Brivudin bedeutsam.[9]
- Mit Datum vom 12. Mai 2020 erschien ein weiterer Rote-Hand-Brief mit folgendem Inhalt: „Es können Todesfälle infolge einer Arzneimittelwechselwirkung zwischen Brivudin und Fluoropyrimidinen (z. B. Fluorouracil (5-FU), Capecitabin, Tegafur, Flucytosin) auftreten. Nach Abschluss der Brivudin-Behandlung muss eine mindestens vierwöchige Wartezeit, eingehalten werden, bevor die Behandlung mit einem Fluoropyrimidin begonnen werden kann. In vielen Fällen kam es zu Todesfällen, wenn diese vierwöchige Wartezeit nicht eingehalten wurde (z. B. wurde Brivudin zwischen zwei 5-FU-Zyklen eingenommen).“[10]
- Verdrängung von Brivudin aus der Plasmaeiweißbindung durch andere Medikamente mit ebenfalls starker Eiweißbindung.
Kontraindikationen[Bearbeiten | Quelltext bearbeiten]
- Schwangerschaft und Stillzeit
- gleichzeitige Gabe bzw. Gabe in den letzten vier Wochen von 5-Fluoropyrimidin-haltigen Medikamenten (siehe vorstehend bei Wechselwirkungen und Anwendungsbeschränkungen)[4]
- Immunsuppression[4]
Kreuzresistenz[Bearbeiten | Quelltext bearbeiten]
Eine Kreuzresistenz besteht mit Aciclovir bei Herpes-simplex- und Varicella-Zoster-Viren.
Pharmakokinetik[Bearbeiten | Quelltext bearbeiten]
- Orale Bioverfügbarkeit: 30 % (wegen ausgeprägten First-Pass-Effekts)
- Absorption: 85 %
- Terminale Halbwertszeit: 16 Stunden
- Ausscheidung: hauptsächlich renal, 20 % via Faeces
Brivudin wird nach oraler Gabe fast vollständig enteral resorbiert. Der maximale Plasmaspiegel wird schon nach 1 Stunde erreicht. Mahlzeiten verzögern die Resorption, senken aber die Resorptionsquote selbst nicht. Bei der First-pass-Metabolisierung entsteht zu ca. 65 % der nicht wirksame Metabolit Bromovinyluracil (BVU). Diese unwirksame Substanz entsteht durch das Enzym Pyrimidinphosphorylase, das die Zuckerkomponente abspaltet. Brivudin wird zu über 95 % an Plasmaproteine gebunden, das Verteilungsvolumen beträgt 75 Liter. Bei einer eingeschränkten Nierenfunktion kommt es zu einer deutlichen Verlängerung der Halbwertszeit.
Weblinks[Bearbeiten | Quelltext bearbeiten]
- Brivudin, Stiftung Warentest, 1. April 2022
Handelsnamen[Bearbeiten | Quelltext bearbeiten]
- Brivex (Schweiz)
- Mevir (Österreich)
- Zostex, Brivudin Aristo (Deutschland, Österreich)
- Zostergalen (Deutschland)[11]
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ Eintrag zu Brivudin. In: Römpp Online. Georg Thieme Verlag, abgerufen am 27. Juni 2019.
- ↑ Datenblatt (E)-5-(2-Bromovinyl)-2′-deoxyuridine bei Sigma-Aldrich, abgerufen am 17. Dezember 2012 (PDF).
- ↑ Epstein-Barr virus encephalitis after kidney transplantation and successful treatment with brivudine, abgerufen am 11. Juli 2017.
- ↑ a b c Diagnostik und Therapie des Zoster und der Postzosterneuralgie - S2k-Leitlinie. (PDF) In: AWMF. 24. Mai 2019, abgerufen am 5. April 2022.
- ↑ arznei-telegramm (5/2007): Brivudin (Zostex) besser als Aciclovir (Zovirax a.a.)?
- ↑ Kirk R. Wilhelmus: Antiviral treatment and other therapeutic interventions for herpes simplex virus epithelial keratitis. In: The Cochrane Database of Systematic Reviews. Band 1, 9. Januar 2015, S. CD002898, doi:10.1002/14651858.CD002898.pub5, PMID 25879115, PMC 4443501 (freier Volltext).
- ↑ Austria-Codex Fachinformation 2005/2006 zu Mevir®.
- ↑ UAW – Aus Fehlern lernen - Potenziell tödlich verlaufende Wechselwirkung zwischen Brivudin (Zostex®) und 5-Fluoropyrimidinen (PDF; 36 kB), Deutsches Ärzteblatt, Jg. 103, Heft 27, 7. Juli 2006, abgerufen auf der WebSite der AkdÄ.
- ↑ Rote-Hand-Brief von Berlin Chemie / Menarini vom 27. August 2012. (PDF) Abgerufen am 4. September 2012.
- ↑ Gelbe Liste Online: Rote-Hand-Brief zu brivudinhaltigen Arzneimitteln | Gelbe Liste. Abgerufen am 12. Mai 2020.
- ↑ E. Brunner, M. Dassinger, I. Grohmann, B. Jung, A. Kuhlmann, M. Löwe, A. Pfleger, A. Schwinn, C. Selz, S. Sieprath, K. Sy: ROTE LISTE 2022. Hrsg.: Rote Liste® Service GmbH. 62. Auflage. Rote Liste® Service GmbH, Frankfurt am Main 2022, ISBN 978-3-946057-74-1, S. 1421–1422.