Flupirtin
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
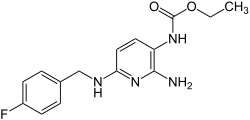
| ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Freiname | Flupirtin | |||||||||||||||||||||
| Andere Namen |
| |||||||||||||||||||||
| Summenformel | C15H17FN4O2 | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code | ||||||||||||||||||||||
| Wirkstoffklasse | ||||||||||||||||||||||
| Wirkmechanismus |
Hemmt die Schmerzweiterleitung durch Stabilisierung des Ruhemembranpotentials[1][2] | |||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 304,32 g·mol−1 | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Flupirtin ist ein Arzneistoff aus der Gruppe der zentral wirkenden, nicht-opioiden Analgetika. Es wirkt sowohl schmerzstillend (analgetisch) als auch muskelentspannend.
Flupirtin war zugelassen zur Behandlung von akuten Schmerzen bei Erwachsenen, wenn eine Behandlung mit anderen Analgetika kontraindiziert ist.[4] Nachdem der Pharmakovigilanz-Ausschuss (PRAC) der Europäischen Arzneimittel-Agentur (EMA) im Februar 2018 empfohlen hatte, aufgrund des hepatotoxischen Potentials die Zulassung von Arzneimitteln mit Flupirtin zu widerrufen,[5][6] nahmen die Anbieter ihre Präparate in den entsprechenden EU-Ländern vom Markt.
Pharmakologie[Bearbeiten | Quelltext bearbeiten]
Flupirtin greift als zentral wirksames Analgetikum an der postsynaptischen Membran an. Es wirkt nicht über eine Beeinflussung der Glutamat-Ausschüttung/Übertragung wie die Opioide, sondern öffnet selektiv einwärtsgerichtete Kaliumkanäle („GIRK“, G-Protein regulated inwardly rectifying K+ channels) an der postsynaptischen Membran.[1] Dadurch stabilisiert sich das Ruhemembranpotential, so dass die Schmerzweiterleitung gehemmt ist. Es bedarf eines größeren Schmerzreizes und dadurch einer erhöhten Glutamat-Ausschüttung, um an der postsynaptischen Membran ein Aktionspotential auszulösen und so den Schmerz weiterzuleiten.[2]
Die muskelentspannende Wirkung beruht auf dem gleichen Prinzip.[7] Allerdings ist nicht sicher, ob nicht noch ein weiterer, bisher unbekannter Mechanismus zur Analgesie existiert.[7]
Die analgetische Potenz von Flupirtin liegt etwa zwischen der von Codein und Morphin.[2]
Nebenwirkungen[Bearbeiten | Quelltext bearbeiten]
Die häufigsten Beschwerden sind Müdigkeit und Schwindel, außerdem können gastrointestinale Beschwerden wie Sodbrennen, Übelkeit oder Durchfall auftreten. Sehr selten kommt es zur arzneimittelinduzierten Hepatitis bis hin zum Leberversagen.[8] Allergische Reaktionen wie Hautausschlag oder Hautjucken (Pruritus) sind möglich. In Einzelfällen kann die Einnahme von Flupirtin zur Abhängigkeitsentwicklung führen.[9]
Die Arzneimittelkommission der deutschen Ärzteschaft (AKdÄ) berichtete im November 2007 über Leberschäden unter Flupirtin.[10] Die Europäische Arzneimittelagentur (EMA) startete im März 2013 ein Risikobewertungsverfahren zu Flupirtin. Das Verfahren ging auf einen Antrag des Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM) zurück, dem insgesamt rund 950 Berichte über unerwünschte Arzneimittelwirkungen vorlagen. Darüber hinaus sah das BfArM die Wirksamkeit von Flupirtin bei chronischen Schmerzen als unzureichend belegt an.[11] In der Folge wurden im Juli 2013 nach Bewertung des Lebertoxizitätsrisikos die therapeutische Anwendung hinsichtlich Zielgruppe und Behandlungsdauer (auf zwei Wochen) eingeschränkt und weitere Maßnahmen angeordnet, um das Risiko von schwerwiegenden Leberschädigungen zu vermindern. Hierzu zählte u. a. die Anforderung wöchentlicher Leberwertekontrollen.[4][12]
Im Oktober 2017 wurde ein erneutes Risikobewertungsverfahren gestartet, da die 2013 beschlossenen Maßnahmen in der Praxis nur unzureichend umgesetzt worden waren und weiterhin Fälle von Leberschäden berichtet wurden.[13] Daraufhin wurde im Februar 2018 von der EMA die Rücknahme der Marktzulassungen empfohlen, da das Risiko für die Patienten überwiege und therapeutische Alternativen verfügbar seien.[5][14] Der Widerruf erfolgte in Deutschland im April 2018.[15] Neben Deutschland sind die Länder des Baltikums, Luxemburg, Polen, Portugal und die Slowakei von der EMA-Empfehlung betroffen.[16]
Wechselwirkungen und Anwendungsbeschränkungen[Bearbeiten | Quelltext bearbeiten]
Flupirtin bindet stark an Serumeiweiße und vermag andere eiweißgebundene Arzneistoffe aus ihrer Bindung zu verdrängen, insbesondere Warfarin und Diazepam, deren Wirkung dadurch verstärkt wird. Auch die Wirkung von Alkohol, muskelentspannenden und weiteren sedierend wirkenden Arzneistoffen kann verstärkt werden.
Flupirtin wird in erheblichem Umfang über die Leber verstoffwechselt, was bei der gleichzeitigen Anwendung von Stoffen mit bekannter und klinisch bedeutsamer Hepatotoxizität (z. B. Carbamazepin, Paracetamol, Alkohol) zu berücksichtigen ist.
Geschichte[Bearbeiten | Quelltext bearbeiten]
Flupirtin wurde von dem Chemiker Walter von Bebenburg für die Firma Asta Medica AG (Frankfurt a. M.) entwickelt. Bebenburg wurde unter seinem Pseudonym Walter E. Richartz als Schriftsteller bekannter.[17]
Handelsnamen[Bearbeiten | Quelltext bearbeiten]
Flupirtin gab es als Monopräparat in Kapseln zu je 100 mg Flupirtinmaleat oder als Retard-Formulierung mit 400 mg Flupirtinmaleat.
Katadolon S long (D), Katadolon (D), Trancolong (D), Trancopal Dolo (D), Flupigil (D), Antidol (A), diverse Generika (D) – alle außer Handel (a.H.).
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ a b J. Kornhuber, S. Bleich, J. Wiltfang, M. Maler, C. G. Parsons: Flupirtine shows functional NMDA receptor antagonism by enhancing Mg2+ block via activation of voltage independent potassium channels. In: J. Neural Transm. Band 106, Nr. 9–10, 1999, S. 857–867, PMID 10599868, doi:10.1007/s007020050206
- ↑ a b c T. Herdegen: Kurzlehrbuch Pharmakologie und Toxikologie. Thieme, Stuttgart / New York 2008, Seite 287.
- ↑ a b Datenblatt Flupirtine maleate salt bei Sigma-Aldrich, abgerufen am 17. Juli 2017 (PDF).
- ↑ a b Flupirtinhaltige Arzneimittel: Umsetzung des Durchführungsbeschlusses der EU-Kommission. BfArM, 27. Januar 2014, archiviert vom am 22. Dezember 2017; abgerufen am 17. Juli 2017.
- ↑ a b PRAC recommends that the marketing authorisation of the painkiller flupirtine be withdrawn. (PDF; 69 kB) Europäische Arzneimittel-Agentur, 9. Februar 2018, abgerufen am 15. Februar 2018 (englisch).
- ↑ Mathias Schneider: Hersteller nehmen Flupirtin-haltige Arzneimittel vom Markt. In: DAZ.online. 21. Februar 2018 (deutsche-apotheker-zeitung.de [abgerufen am 15. März 2018]).
- ↑ a b M. Strohmeier: Flupirtin: Wirkung, Anwendungsgebiete, Nebenwirkungen. 19. Januar 2019, abgerufen am 22. März 2020.
- ↑ Fachinformation Katadolon 100 mg Hartkapseln, Stand Oktober 2008, AWD.pharma GmbH & Co. KG. Abrufbar auf dem Portal des Bundes und der Länder, PharmNet.Bund
- ↑ C. Stoessel, A. Heberlein, T. Hillemacher, S. Bleich, J. Kornhuber: Positive reinforcing effects of flupirtine--two case reports. In: Progress in Neuro-Psychopharmacology & Biological Psychiatry. Band 34, Nr. 6, 2010, S. 1120–1121, doi:10.1016/j.pnpbp.2010.03.031, PMID 20362025.
- ↑ Leberschäden unter Flupirtin (PDF; 127 kB) Aus der UAW-Datenbank der Arzneimittelkommission der deutschen Ärzteschaft (AKdÄ), Veröffentlicht im Deutschen Ärzteblatt am 16. November 2007, zuletzt abgerufen am 26. Oktober 2021.
- ↑ Flupirtin: Europäisches Risikobewertungsverfahren gestartet. BfArM, 15. März 2013, archiviert vom am 22. Dezember 2017; abgerufen am 17. Juli 2017.
- ↑ Arzneimittelkommission der deutschen Ärzteschaft (AkdÄ): Rote-Hand-Brief Einschränkung der therapeutischen Zielgruppe und Begrenzung der Behandlungsdauer nach Bewertung des Lebertoxizitätsrisikos, (PDF; 369 kB).
- ↑ Flupirtin: Schwerwiegende Leberschäden., BfArM, 24. Mai 2018.
- ↑ Drug Safety Mail 2018-08 – Information der EMA zu Flupirtin-haltigen Arzneimitteln: PRAC empfiehlt Rücknahme der Marktzulassung. AkdÄ, 9. Februar 2018, abgerufen am 10. Februar 2018.
- ↑ Flupirtin: Rückruf und Widerruf der Zulassung des Schmerzmittels Flupirtin, Meldung der AKDAE vom 5. Juni 2018, abgerufen am 22. Juni 2018.
- ↑ Endlich: Aus für Flupirtin in Sicht ... a-t fordert von den Anbietern sofortige eigenverantwortliche Marktrücknahme, arznei-telegramm, 16. Februar 2018.
- ↑ Heribert Offermanns: W.E. Richartz, W. von Bebenburg – Schriftsteller und Chemiker. In: Chemie in unserer Zeit. Band 46, Nr. 3, 2012, S. 158–159, doi:10.1002/ciuz.201200591.