Freund-Reaktion
Die Freund-Reaktion ist eine Reaktion der Organischen Chemie und wurde 1881 von dem galizischen Chemiker August Freund (1835–1892) entdeckt. Sie dient zur Synthese von Cyclopropan (Trimethylen) und seinen Derivaten und ähnelt der intramolekularen Wurtzschen Synthese.[1][2]
Übersichtsreaktion[Bearbeiten | Quelltext bearbeiten]
Freund experimentierte zunächst mit 1,3-Dibrompropan und Natrium, woraus er Cyclopropan gewinnen konnte:[3][4]
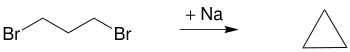
Analog wie 1,3-Dibrompropan reagieren 1,3-Dichlor- und 1,3-Diiodpropan. Durch die Analyse des Produkts, das Freund Trimethylen nannte, und einem Ausschlussverfahren konnte er die korrekte Struktur von Cyclopropan aufstellen, sodass Freund für seine Cyclopropansynthese bekannt wurde.[3]
Modifikation[Bearbeiten | Quelltext bearbeiten]
Gustavson-Reaktion[Bearbeiten | Quelltext bearbeiten]
In der Gustavson-Reaktion wird statt Natrium Zinkstaub in der Cyclisierungsreaktion eingesetzt.
Hass-Cyclopropan-Prozess[Bearbeiten | Quelltext bearbeiten]
Um weiterhin Abstand zur Wurtzschen Synthese zu gewinnen und die Ausbeuten zu verbessern, modifizierte 1931 Henry Bohn Hass (1902–1987) die Reaktion durch das Verwenden von Zinkstaub, verdünnten Alkohol und einer katalytischen Menge von Natriumiodid.[1]
Mechanismus[Bearbeiten | Quelltext bearbeiten]
Der Mechanismus gleicht dem Mechanismus der Wurtzschen Synthese. Diese kann sowohl radikalisch, als auch über anionische Zwischenstufen verlaufen.[5] Anhand der Reaktion zwischen 1,3-Dibrompropan 1 und Natrium soll der noch nicht vollständig bewiesene Mechanismus der Freund-Reaktion erklärt werden:

Im ersten Schritt greift das Natrium mit seinem freien Elektron die C-Br-Bindung an, sodass Natriumbromid abgespalten wird und ein Brompropyl-Radikal 2 zurückbleibt. Mit weiterem Natrium entsteht ein Natriumsalz 3, bestehend aus halogeniertem Carbanion und Natrium-Kation. Das negativ geladene Kohlenstoffatom des Anions greift nukleophil das Kohlenstoff, an dem sich das Brom-Atom befindet, an. Währenddessen greift das Brom mit einer seinen freien Elektronenpaarbindungen, unter Mitnahme der Elektronenpaarbindung zum Kohlenstoff-Atom, das Natrium-Kation an. Es bildet sich durch diesen Ringschluss Cyclopropan 4.
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ a b Zerong Wang: Comprehensive Organic Name Reactions and Reagents. John Wiley & Sons, 2009, ISBN 978-0-471-70450-8, S. 1123–1125.
- ↑ H. F. Ebel, A. Lüttringhaus, Houben-Weyl: Methoden der Organischen Chemie. 4. Auflage. Thieme, Stuttgart 1970, ISBN 3-13-212904-6, S. 492.
- ↑ a b August Freund: Über Trimethylen. In: Journal für Praktische Chemie. Band 26, Nr. 1, 1882, S. 367–377, doi:10.1002/prac.18820260125.
- ↑ August Freund: Über Trimethylen. In: Monatshefte für Chemie. Band 3, Nr. 1, 1881, S. 625–635, doi:10.1007/BF01516828.
- ↑ Zerong Wang: Comprehensive Organic Name Reactions and Reagents. John Wiley & Sons, 2009, ISBN 978-0-471-70450-8, S. 3094–3099.