Tetraphenylblei
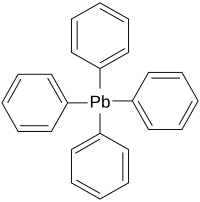
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Tetraphenylblei | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C24H20Pb | |||||||||||||||
| Kurzbeschreibung |
weißes Pulver[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 515,62 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest[1] | |||||||||||||||
| Dichte |
1,53 g·cm−3[2] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt |
325 °C[2] | |||||||||||||||
| Löslichkeit | ||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Tetraphenylblei ist eine chemische Verbindung aus der Gruppe der organischen Bleiverbindungen. Der weiße Feststoff ist in organischen Lösemitteln relativ gut, in Wasser nahezu unlöslich.
Gewinnung und Darstellung[Bearbeiten | Quelltext bearbeiten]
Über die Darstellung von Tetraphenylblei durch Umsetzung des Grignard-Reagenz Phenylmagnesiumbromid mit Blei(II)-chlorid in Diethylether wurde zuerst 1904 von P. Pfeiffer und P. Truskier berichtet.[4]
Eigenschaften[Bearbeiten | Quelltext bearbeiten]
Durch Umsetzung von Tetraphenylblei mit alkoholischer Chlorwasserstoff-Lösung lassen sich unter Bildung von Benzol sukzessive Phenylgruppen durch Chloridionen ersetzen:[5]
Wie das homologe Tetrabutylblei reagiert auch Tetraphenylblei mit elementarem Schwefel bei Temperaturen über 150 °C explosionsartig unter Bildung von Diphenylsulfid und Bleisulfid:[6]
Verwendung[Bearbeiten | Quelltext bearbeiten]
Durch Reaktion mit Iod in Chloroform kann Triphenylbleiiodid gewonnen werden.[7]
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ a b c d e Datenblatt Tetraphenyllead, 97% bei Alfa Aesar, abgerufen am 10. November 2021 (Seite nicht mehr abrufbar).
- ↑ a b c Datenblatt Tetraphenyllead, min. 97% (PDF) bei Strem, abgerufen am 18. Juni 2023.
- ↑ Walter Strohmeier, Karlheinz Miltenberger: Notiz über die Löslichkeiten von Tetraphenylmethan Tetraphenyl-silicium, -germanium, -zinn und -blei in organischen Lösungsmitteln. In: Chemische Berichte. Band 91, Nr. 6, Juni 1958, S. 1357, doi:10.1002/cber.19580910638.
- ↑ P. Pfeiffer, P. Truskier: Zur Darstellung organischer Blei- und Quecksilber-Verbindungen. In: Berichte der deutschen chemischen Gesellschaft. Band 37, Nr. 1, Januar 1904, S. 1125, doi:10.1002/cber.190403701183.
- ↑ F. Just: Chemisches Colloquium der Universität Berlin. In: Angewandte Chemie. Band 59, Nr. 5-6, Mai 1947, S. 176, doi:10.1002/ange.19470590510 (Originaltitel: Untersuchungen über blei- und zinnorganische Verbindungen.).
- ↑ Max Schmidt, Herbert Schumann: Spaltungsreaktionen metallorganischer Verbindungen mit Chalkogenen. Reaktionen von Schwefel mit silicium-, germanium- und bleiorganischen Verbindungen. In: Zeitschrift für anorganische und allgemeine Chemie. Band 325, Nr. 3-4, Oktober 1963, S. 130, doi:10.1002/zaac.19633250305.
- ↑ Richard W. Weiss: Compounds of Germanium, Tin, and Lead, including Biological Activity and Commercial Application Covering the Literature from 1937 to 1964. Springer Science & Business Media, 2013, ISBN 978-3-642-51889-8, S. 555 (eingeschränkte Vorschau in der Google-Buchsuche).
- Stoff mit reproduktionstoxischer Wirkung
- Gesundheitsschädlicher Stoff (Organschäden)
- Umweltgefährlicher Stoff (chronisch wassergefährdend)
- Gesundheitsschädlicher Stoff bei Verschlucken
- Gesundheitsschädlicher Stoff bei Einatmen
- Phenylsubstituierte Verbindung
- Bleiorganische Verbindung
- Beschränkter Stoff nach REACH-Anhang XVII, Eintrag 63
- Beschränkter Stoff nach REACH-Anhang XVII, Eintrag 72



![{\displaystyle \mathrm {(C_{6}H_{5})MgBr+\ 2\ PbCl_{2}\ {\xrightarrow[{Et_{2}O}]{}}\ Pb(C_{6}H_{5})_{4}+\ Pb+\ 4\ MgBrCl} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/a68a002fb9900cd1c48b06092065ba8cde358c05)
![{\displaystyle \mathrm {Pb(C_{6}H_{5})_{4}+\ HCl\ {\xrightarrow[{Ethanol}]{}}\ Pb(C_{6}H_{5})_{3}Cl+\ C_{6}H_{6}} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/2417302affebdbea4b3f34bc6fc75d673f1ad62d)
![{\displaystyle \mathrm {Pb(C_{6}H_{5})_{3}Cl+\ HCl\ {\xrightarrow[{Ethanol}]{}}\ Pb(C_{6}H_{5})_{2}Cl_{2}+\ C_{6}H_{6}} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/5fbdfb1f11bde306d1775ec460db04f257f26fd8)
![{\displaystyle \mathrm {Pb(C_{6}H_{5})_{4}+\ 3\ S\ {\xrightarrow[{}]{}}\ PbS+\ 2\ S(C_{6}H_{5})_{2}} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/aa19921cfbe9c8890ff58c0053fbc5c037b79041)