Tosylaminohexansäure
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|

| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Tosylaminohexansäure | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C13H19NO4S | ||||||||||||||||||
| Kurzbeschreibung |
weißes kristallines Pulver[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 285,36 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Dichte |
1,175 g·cm−3[2] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Löslichkeit | |||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Tosylaminohexansäure vereint Strukturelemente eines Sulfonamids und einer Aminosäure und wird durch Umsetzung von ε-Aminocapronsäure mit para-Toluolsulfonsäurechlorid erhalten. Sie wird, insbesondere in Form ihres Triethanolamin-Salzes,[5] als Korrosionsschutzmittel in wässrigen Systemen verwendet.
Darstellung[Bearbeiten | Quelltext bearbeiten]
Die Umsetzung von 6-Aminohexansäure mit Tosylchlorid in alkalischem (pH ca. 11) Wasser/1,4-Dioxan-Gemisch liefert nach Ansäurern Tosylaminohexansäure, die zur Reinigung aus 40%igem Ethanol umkristallisiert werden kann,[1]

oder eine Lösung von Tosylchlorid in Tetrahydrofuran wird zu einer Lösung von ε-Aminocapronsäure in 1M Natronlauge gegeben und bei pH 11 unter Bildung von p-Toluolsulfonyl-ε-aminocapronsäure in 94%iger Ausbeute zur Reaktion gebracht.[3]
Eigenschaften[Bearbeiten | Quelltext bearbeiten]
Tosylaminohexansäure ist ein weißer kristalliner Feststoff, der in Wasser bei neutralem pH-Wert kaum, in alkalischem pH gut löslich ist. Die Säure besitzt ein geringes Wassergefährdungspotential.[5] und ist mit anderen Korrosionsinhibitoren sehr gut verträglich.
Verwendung[Bearbeiten | Quelltext bearbeiten]
6-(N-Tosylamino)capronsäure ist ein so genannter aschefreier und wenig schäumender Inhibitor für die Korrosion von Eisen und Eisen-Legierungen in wässrigen Systemen und wird meist als Triethanolamin-Salz in Konzentrationen von 0,2 bis 2,5 % Wirkstoffgehalt eingesetzt.[5]
Tosylaminohexansäure auch in Systemen mit mehreren Metallen ein hochwirksamer Korrosionsinhibitor. Die Verbindung – insbesondere als Salz mit Triethanolamin, das ebenfalls antikorrosive Eigenschaften hat – vermindert die Korrosivität wasserhaltiger Kühl- und Hydraulikflüssigkeiten[6], Metallbearbeitungs-[7] und -reinigungsflüssigkeiten[8] und von Kühlschmiermitteln[9], wie Bohr- und Schneidemulsionen (engl. metal working fluids) und leistet Korrosionsschutz beim Drahtziehen sowie bei Offshore-Anwendungen.
Das von Tosylaminohexansäure abgeleitete Chlormethylketon[10]
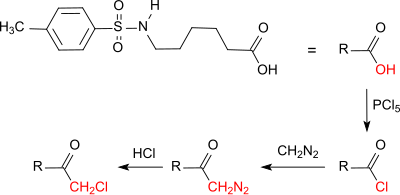
zeigte im Tiermodell Ehrlich Ascites Carcinoma[11] (experimenteller Mäusetumor) hohe antineoplastische Aktivität.
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ a b c B. Benacerraf, B.B. Levine: Immunological specificity of delayed and immediate hypersensitivity reactions. In: J. Exptl. Med. Band 115, Nr. 5, 1962, S. 1023–1036, doi:10.1084/jem.115.5.1023, PMC 2137528 (freier Volltext).
- ↑ a b c d Eintrag zu 6-(((4-Methylphenyl)sulfonyl)amino)hexansäure in der GESTIS-Stoffdatenbank des IFA, abgerufen am 17. November 2022. (JavaScript erforderlich)
- ↑ a b V.H. Pavlidis, E.D. Chan, L. Pennington, M. McParland, M. Whitehead, I.G.C. Coutts: Synthesis of aliphatic amines related to monodansylcadaverine via the oxidative rearrangement of aliphatic amides with phenyl iodosyl bis(trifluoroacetate). In: Synth. Commun. Band 18, Nr. 14, 1988, S. 1615–1624, doi:10.1080/00397918808081322.
- ↑ Patent US3788991: Metal working agents. Angemeldet am 24. Januar 1972, veröffentlicht am 29. Januar 1974, Anmelder: Farbwerke Hoechst AG, Erfinder: H. Diery, S. Rittner, H. Lorke.
- ↑ a b c Metall-Chemie, Produktdatenblatt TC® 50, (Online).
- ↑ Patent US8759264B2: Water-based hydraulic fluids comprising dithio-di(aryl carboxylic acids). Angemeldet am 2. Dezember 2009, veröffentlicht am 24. Juni 2014, Anmelder: Clariant Finance (BVI) Ltd., Erfinder: R. Kupfer, C. Cohrs.
- ↑ Patent US20120088706A1: Water-mixed metal working fluids containing ether pyrrolidone carboxylic acids. Angemeldet am 19. Mai 2010, veröffentlicht am 12. April 2012, Anmelder: Clariant Finance (BVI) Ltd., Erfinder: R. Kupfer, C. Cohrs, A. Roesch.
- ↑ Patent WO0031218: Metallbearbeitungs- und Reinigungsverfahren. Angemeldet am 17. November 1999, veröffentlicht am 1. Juni 2000, Anmelder: Henkel KGaA, Erfinder: J. Geke, B. Stedry, W. Klose.
- ↑ Patent US20120088705A1: Polyalkylene glycol-based ether pyrrolidone carboxylic acids, and concentrates for the production of synthetic cooling lubricants containing the same. Angemeldet am 19. Mai 2010, veröffentlicht am 12. April 2012, Anmelder: Clariant Finance (BVI) Ltd., Erfinder: R. Kupfer, C. Cohrs, A. Roesch.
- ↑ Z. Sajadi, M. Kashani, L.J. Loeffler, I.H. Hall: Antitumor agents: Diazomethyl ketone and chloromethyl ketone analogues prepared from N-tosyl amino acids. In: J. Med. Chem. Band 23, Nr. 3, 1980, S. 275–278, doi:10.1021/jm00177a012.
- ↑ M. Ozaslan, I.D. Karagoz, I.H. Kilic, M.E. Guldur: Review: Ehrlich ascites carcinoma. In: Afr. J. Biotechnol. Band 10, Nr. 13, 2011, S. 2375–2378, doi:10.5897/AJBx10.017.