3-Methyl-1,2-butadien
Zur Navigation springen
Zur Suche springen
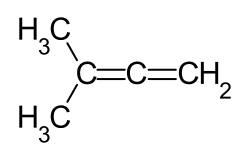
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | 3-Methyl-1,2-butadien | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C5H8 | |||||||||||||||
| Kurzbeschreibung |
farblose Flüssigkeit[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 68,12 g·mol−1 | |||||||||||||||
| Aggregatzustand |
flüssig[1] | |||||||||||||||
| Dichte |
0,694 g·cm−3 (25 °C)[1] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt |
40–41 °C[1] | |||||||||||||||
| Dampfdruck | ||||||||||||||||
| Löslichkeit |
löslich in Diethylether, Benzol, Aceton und Ethanol[2] | |||||||||||||||
| Brechungsindex |
1,419 (20 °C)[1] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | ||||||||||||||||
3-Methyl-1,2-butadien ist eine chemische Verbindung aus der Gruppe der Alkadiene.
Gewinnung und Darstellung[Bearbeiten | Quelltext bearbeiten]
3-Methyl-1,2-butadien kann durch Reaktion von 1,1-Dichlor-2-ethoxy-3,3-dimethylcyclopropan mit Methyllithium und Diethylether gewonnen werden.[3][4]
Eigenschaften[Bearbeiten | Quelltext bearbeiten]
3-Methyl-1,2-butadien ist eine farblose Flüssigkeit, die löslich in Diethylether, Benzol, Aceton und Ethanol ist.[2]
Verwendung[Bearbeiten | Quelltext bearbeiten]
3-Methyl-1,2-butadien wird verwendet, um die photoinduzierte Reaktion mit den Cyanoarenen 1,2,4,5-Tetracyanbenzol, 1,4-Dicyanbenzol und 1,4-Dicyanonaphthalin in Gegenwart von Methanol als Nukleophil zu untersuchen.[2]
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ a b c d e f g h i Datenblatt 3-Methyl-1,2-butadiene, 97% bei Sigma-Aldrich, abgerufen am 12. August 2019 (PDF).
- ↑ a b c Datenblatt 3-Methyl-1,2-butadiene, 97+% bei Alfa Aesar, abgerufen am 12. August 2019 (Seite nicht mehr abrufbar).
- ↑ Lars Skattebøl: Chemistry of gem-Dihalocyclopropanes. IV. Ring Opening of gem-Dichlorocyclopropyl Ethers. In: The Journal of Organic Chemistry. 31, 1966, S. 1554–1559, doi:10.1021/jo01343a057.
- ↑ PrepChem.com: Synthesis of 3-methylbuta-1,2-diene - PrepChem.com, accessdate: 12. August 2019.


