Anthranil
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
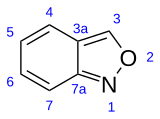
| |||||||||||||||||||
| Strukturformel mit Lokanten | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Anthranil | ||||||||||||||||||
| Andere Namen | |||||||||||||||||||
| Summenformel | C7H5NO | ||||||||||||||||||
| Kurzbeschreibung |
farblose Flüssigkeit[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 119,04 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
flüssig[1] | ||||||||||||||||||
| Dichte |
1.183 g·cm−3 (bei 25 °C)[1] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt | |||||||||||||||||||
| Löslichkeit |
| ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Anthranil (systematisch 2,1-Benzoxazol) ist eine chemische Verbindung aus der Gruppe der Heterocyclen, genauer der Azole. Der Trivialname leitet sich von der strukturverwandten Anthranilsäure ab. Systematisch betrachtet ist es eines der drei möglichen Benzoxazole; die anderen sind 1,2-Benzoxazol (Indoxazen) und 1,3-Benzoxazol.
Gewinnung und Darstellung[Bearbeiten | Quelltext bearbeiten]
Anthranil kann, wie von Paul Friedlaender und Robert Henriques 1882 gezeigt, aus 2-Nitrobenzaldehyd synthetisiert werden. Dazu wird das Edukt in der 3-fachen Menge Essigsäure gelöst, leicht erwärmt und Zinnpulver portionsweise hinzugegeben. Durch die Reaktionswärme kann die Reaktionslösung bei der richtigen Zinn-Zufuhrrate am Kochen erhalten werden. Zur Isolation des Produktes muss die Reaktionslösung mit Natriumcarbonat neutralisiert werden und eine Wasserdampfdestillation angefügt werden.[2]
Eigenschaften[Bearbeiten | Quelltext bearbeiten]
Physikalische Eigenschaften[Bearbeiten | Quelltext bearbeiten]
- Flammpunkt im geschlossenen Tiegel: 94 °C[1]
- Verteilungskoeffizient n-Octanol/Wasser: 1,824[1]
Chemische Eigenschaften[Bearbeiten | Quelltext bearbeiten]
Anthranil ist an der Luft nicht stabil. Es färbt sich nach einiger Zeit braun und polymerisiert. Mit Quecksilber(II)-chlorid in wässriger Lösung bildet sich ein Niederschlag in Form von feinen Kristallnadeln. Mit Alkalien, Ammoniak, oder kochendem Wasser entsteht durch Addition von Wasser die Anthranilsäure. Durch Reduktion entsteht 2-Aminobenzaldehyd.[3][2]
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ a b c d e f g h Datenblatt Anthranil bei Sigma-Aldrich, abgerufen am 11. Mai 2022 (PDF).
- ↑ a b c d e f P. Friedländer, R. Henriques: Zur reduktion des orthonitrobenzaldehyds. In: Berichte der deutschen chemischen Gesellschaft. Band 15, Nr. 2, 1882, S. 2105–2110, doi:10.1002/cber.188201502147.
- ↑ Externe Identifikatoren von bzw. Datenbank-Links zu 2-Aminobenzaldehyd: CAS-Nummer: 529-23-7, EG-Nummer: 208-454-3, ECHA-InfoCard: 100.007.687, PubChem: 68255, ChemSpider: 61553, Wikidata: Q21099244.
