Nickelselenid
| Kristallstruktur | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
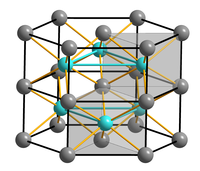
| ||||||||||||||||
| _ Ni3+ _ Se3− | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Nickelselenid | |||||||||||||||
| Andere Namen |
Nickelmonoselenid | |||||||||||||||
| Verhältnisformel | NiSe | |||||||||||||||
| Kurzbeschreibung |
grauer geruchloser Feststoff[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 137,65 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest[1] | |||||||||||||||
| Dichte |
8,46 g·cm−3 (20 °C)[1] | |||||||||||||||
| Löslichkeit |
praktisch unlöslich in Wasser[1] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Nickelselenid ist eine anorganische chemische Verbindung des Nickels aus der Gruppe der Selenide. Die Verbindung weist eine Phasenbreite bis zu Ni3Se4 auf und ist neben Ni3Se2, NiSe2 und möglicherweise weiteren existierende Phasen nur eines der Nickelselenide.[3]
Vorkommen[Bearbeiten | Quelltext bearbeiten]
Die β-Form von Nickelselenid kommt natürlich in Form des Minerals Sederholmit vor, die γ-Form als Mäkinenit. Auch die anderen Nickelselenide kommen natürlich vor. So entspricht Wilkmanit der monoklinen Ni3Se4-Phase, Kullerudit und Penroseit (beide NiSe2) sind die orthorhombischen beziehungsweise kubischen Nickelanalogon von Ferroselit (FeSe2) und Trüstedtit Ni3Se4 ist ein kubischer Spinell.[4]
Gewinnung und Darstellung[Bearbeiten | Quelltext bearbeiten]
Nickelselenid kann durch Einleiten von Selenwasserstoff in eine mit Natriumacetat versetzte Nickelsalzlösung gewonnen werden, wobei die schwarze amorphe Form entsteht, die stets etwas Selen enthält.[5]
Unter Luftabschluss fällt aus neutraler wässriger Nickelsalzlösung mit Ammoniumselenid die amorphe α-Form aus, aus essigsaurer Nickelacetatlösung mit Selenwasserstoff die hexagonale β-Form und aus schwefelsaurer Nickelsulfatlösung mit Selenwasserstoff die instabile rhomboedrische γ-Form. Diese tritt nur unter 32 °C und neben der β-Form und Ni3Se2 auf.[3]
Dünne Schichten können auch direkt durch Reaktion von glühendem Nickel mit Selendampf gewonnen werden.[3]
Eine Reihe von Nickelseleniden (NiSe und NiSe2) können durch Reaktion von Selen(IV)-chlorid mit Nickel(II)-chloridhexahydrat in Gegenwart von Cetyltrimethylammoniumbromid (CTAB) als Tensid und Hydrazinhydrat als Reduktionsmittel bei 180 °C synthetisiert werden.[6]
Eigenschaften[Bearbeiten | Quelltext bearbeiten]
Nickelselenid ist ein grauer geruchloser Feststoff, der praktisch unlöslich in Wasser ist.[1] Es ist in kalten wie erhitzten verdünnten Mineralsäuren nicht löslich, mit konzentrierter Salzsäure entwickelt es nach und nach Selenwasserstoff.[5] Es ist vollständig löslich in Königswasser und unlöslich in Alkalien.[3] Im trockenen Zustande verändert es sich nur langsam unter Oxidation, wobei teilweise NiSeO3 entsteht. Dagegen zeigt es keine Neigung zur Bildung von kolloidalen Lösungen, wie dies beim Nickel(II)-sulfid der Fall ist.[5]
Die β-Form besitzt eine hexagonale Kristallstruktur vom Nickelarsenidtyp mit der Raumgruppe P63/mmc (Raumgruppen-Nr. 194).[3] Dagegen hat Ni3Se2 eine rhombohedrale Kristallstruktur mit der Raumgruppe R32 (Raumgruppen-Nr. 155).[7]
Verwendung[Bearbeiten | Quelltext bearbeiten]
Nickel-Selenid-Dünnschichten sind wichtige Halbleitermaterialien und könnten als absorbierenden Materialien in photoelektrochemischen Zellen verwendet werden.[8]
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ a b c d e f g Eintrag zu Nickelselenid in der GESTIS-Stoffdatenbank des IFA, abgerufen am 8. Januar 2020. (JavaScript erforderlich)
- ↑ Eintrag zu Nickel selenide im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. August 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- ↑ a b c d e R. J. Meyer: Nickel Teil B – Lieferung 2. Verbindungen bis Nickel-Polonium. Springer-Verlag, 2013, ISBN 978-3-662-13302-6, S. 745 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Sederholmite, Wilkmanite, Kullerudite, Makinenite and Trustedtite, five new nickel selenide minerals by Y. Vuorelainen, A. Huhma and A. Häkli Outokumpu co., Finnland, abgerufen am 29. Juni 2016
- ↑ a b c Ludwig Moser, Kasimir Atynski: Die Darstellung von Seleniden aus Selenwasserstoff und Metallsalzlösungen. In: Monatshefte für Chemie. 45, 1925, S. 235, doi:10.1007/BF01524665.
- ↑ Azam Sobhani, Masoud Salavati-Niasari: Synthesis and characterization of a nickel selenide series via a hydrothermal process. In: Superlattices and Microstructures. Band 65, 1. Januar 2014, S. 79–90, doi:10.1016/j.spmi.2013.10.030.
- ↑ R. P. Agarwala, A. P. B. Sinha: Crystal structure of nickel selenide – Ni3Se2. In: Zeitschrift für anorganische und allgemeine Chemie. 289, 1957, S. 203, doi:10.1002/zaac.19572890117.
- ↑ H.S. Min: Metal selenide semiconductor thin films: A review. Band 9, Nr. 3, 1. Januar 2016 (researchgate.net).

