Vinyltributylzinn
Zur Navigation springen
Zur Suche springen
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
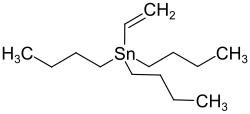
| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Vinyltributylzinn | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C14H30Sn | ||||||||||||||||||
| Kurzbeschreibung |
farblose Flüssigkeit[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 317,10 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
flüssig[1] | ||||||||||||||||||
| Dichte |
1,085 g·cm−3 (25 °C)[1] | ||||||||||||||||||
| Siedepunkt | |||||||||||||||||||
| Löslichkeit |
löslich in Chloroform[2] | ||||||||||||||||||
| Brechungsindex |
1,478 (20 °C)[1] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | |||||||||||||||||||
Vinyltributylzinn ist eine chemische Verbindung aus der Gruppe der zinnorganischen Verbindungen.
Gewinnung und Darstellung[Bearbeiten | Quelltext bearbeiten]
Vinyltributylzinn kann durch Reaktion von Vinylmagnesiumbromid mit Tributylzinnchlorid gewonnen werden.[3] Derivate können durch Pyrolyse von Alkyltributylzinnacetaten bei hohen Temperaturen gewonnen werden.[4]
Eigenschaften[Bearbeiten | Quelltext bearbeiten]
Vinyltributylzinn ist eine farblose Flüssigkeit,[1] die löslich in Chloroform ist.[2]
Verwendung[Bearbeiten | Quelltext bearbeiten]
Vinyltributylzinn kann als Vinyl-Nucleophil für Bromacetylene und Bromaromaten verwendet werden.[1]
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ a b c d e f g h i j k Datenblatt Vinyltributylzinn, 97% bei Sigma-Aldrich, abgerufen am 28. September 2023 (PDF).
- ↑ a b Eintrag zu Tributyl(vinyl)tin bei Toronto Research Chemicals, abgerufen am 29. September 2023 (PDF).
- ↑ Organic Syntheses Procedure - Org. Synth. 1959, 39, 10. In: orgsyn.org. Abgerufen am 29. September 2023 (englisch). doi:10.15227/orgsyn.039.0010
- ↑ J. Georges Duboudin, Michel Petraud, Max Ratier, Bruno Trouve: A new route to vinyltributyltin compounds by flash pyrolysis of alkyltributyltin acetates. In: Journal of Organometallic Chemistry. Band 288, Nr. 1, 1985, S. C6–C8, doi:10.1016/0022-328X(85)80112-1.
Kategorien:
- Feuergefährlicher Stoff
- Beschränkter Stoff nach REACH-Anhang XVII, Eintrag 40
- Giftiger Stoff bei Verschlucken
- Gesundheitsschädlicher Stoff bei Hautkontakt
- Hautreizender Stoff
- Augenreizender Stoff
- Stoff mit reproduktionstoxischer Wirkung
- Gesundheitsschädlicher Stoff (Organschäden)
- Umweltgefährlicher Stoff (chronisch wassergefährdend)
- Alkylzinnverbindung
- Vinylverbindung



