Isopropylnitrit
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
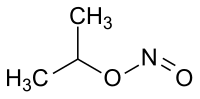
| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Isopropylnitrit | ||||||||||||||||||
| Andere Namen |
2-Propylnitrit | ||||||||||||||||||
| Summenformel | C3H7NO2 | ||||||||||||||||||
| Kurzbeschreibung |
gelbliche, transparente Flüssigkeit[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 89,09 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
flüssig[1] | ||||||||||||||||||
| Dichte |
1,02 g·cm−3[1] | ||||||||||||||||||
| Siedepunkt |
39 °C[1] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Isopropylnitrit (IPN) ist eine chemische Verbindung aus der Gruppe der Alkylnitrite. Es ist eine gelbliche, transparente Flüssigkeit,[1] die bei unvorsichtigem Umgang explodieren kann (Schlagempfindlichkeit).[3]

Darstellung[Bearbeiten | Quelltext bearbeiten]
Isopropylnitrit kann durch die Reaktion von Isopropanol mit Nitrosylchlorid, Salpetriger Säure[4] oder Natriumnitrit/HCl gewonnen werden.[5]
Verwendung[Bearbeiten | Quelltext bearbeiten]
Isopropylnitrit wird als Droge in Form von Poppers verwendet. Heutzutage ist Isopropylnitrit der Hauptbestandteil dieser Produkte, nachdem das früher verwendete Isobutylnitrit aufgrund seiner Karzinogenität in der EU verboten wurde.[6] In Synthesen kann es als Reagens zur Nitrosierung genutzt werden. So kann Phenacylchlorid mit Isopropylnitrit nitrosiert werden.[7] 3-Hydroxy-2-(polyfluoralkyl)chromone lassen sich über eine Nitrosierung von 2-(Polyfluoralkyl)chroman-4-onen herstellen.[8]
Einzelnachweise[Bearbeiten | Quelltext bearbeiten]
- ↑ a b c d e f g Safety Data Sheet: Isopropyl nitrite 95%. Pfaltz&Bauer, 10. Januar 2018, abgerufen am 2. April 2022.
- ↑ a b R. J. Lewis (Ed.): Isopropyl Nitrite 541-42-4. In: Sax's Dangerous Properties of Industrial Materials. 2012, doi:10.1002/0471701343.sdp40876.
- ↑ D. C. H. Bulpitt, D. Noble-Nesbitt, J. Carreira: Effects of exposure to Isopropyl nitrite. In: Occupational Medicine. Band 48, Nr. 5, 1998, S. 345–346, doi:10.1093/occmed/48.5.345.
- ↑ John E. Logsdon, Richard A. Loke: Isopropyl Alcohol. In: Kirk-Othmer Encyclopedia of Chemical Technology. 4. Dezember 2000, doi:10.1002/0471238961.0919151612150719.a01.
- ↑ Shuang Liang Xiaohui Cao, Xilong Yan, Ligong Chen: A Mild and Practical Synthesis of Biphenyl Compounds. In: Journal of Chemical Research. Band 36, Nr. 9, 1. September 2012, S. 555 f., doi:10.3184/174751912X13419099572319.
- ↑ Rachel Brazil: What are poppers and are they legal? In: chemistryworld.com. Royal Society of Chemistry, 16. September 2021, abgerufen am 2. April 2022.
- ↑ Robert Simonoff: FURTHER STUDIES ON THE SYNTHESIS OF ARYLETHANOLAMINS. 1945 (umd.edu [PDF]).
- ↑ Roman A. Irgashev, Vyacheslav Ya. Sosnovskikh, Anna A. Sokovnina, Gerd-Volker Röschenthaler: The first synthesis of 3-hydroxy-2-(polyfluoroalkyl)chromones and their ammonium salts. 3-hydroxychromone in the Mannich reaction. In: Journal of Heterocyclic Chemistry. Band 47, Nr. 4, 10. Juli 2010, S. 944–948, doi:10.1002/jhet.386.
- Feuergefährlicher Stoff
- Beschränkter Stoff nach REACH-Anhang XVII, Eintrag 40
- Gesundheitsschädlicher Stoff bei Verschlucken
- Gesundheitsschädlicher Stoff bei Hautkontakt
- Hautreizender Stoff
- Augenreizender Stoff
- Gesundheitsschädlicher Stoff bei Einatmen
- Atemwegsreizender Stoff
- Synthetische psychotrope Substanz
- Nitrit
- Isopropylester

